Макроскопическая стадия
Cтраница 3
Было установлено, что процесс протекает в две макроскопические стадии: первая - до дозы 1 - Ю19 эв / мл и вторая - при более высоких дозах. На первой чисто радикальной стадии выходы образования формальдегида и перекиси водорода равны 1 9 и 2 3 молекул / 100 эв. [31]
Таким образом, приведенные данные показывают, что первая макроскопическая стадия окисления представляет собой окисление жира, ингибированное либо природным, либо синтетическим ингибитором, а вторая стадия связана с быстрым развитием окислительных процессов после разрушения этих ингибиторов. [32]
Существование в процессе окисления нескольких разделяющихся во времени макроскопических стадий позволяет до-новому поставить вопрос об управлении процессом химического превращения. Процесс, состоящий из нескольких макроскопических стадий, ряде случаев нецелесообразно проводить при неизменных условиях, так как оптимальные условия для различных стадий могут быть существенно различны. Наиболее наглядным примером применения этого положения являются уже рассмотренные опыты по газовому инициированию процессов окисления, в которых один и тот же инициатор ускоряет процесс на ранних стадиях и тормозит его на более глубоки стадиях. [33]
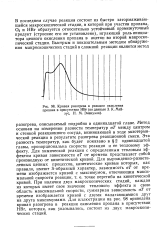 |
Кривая разогрева в реакции окисления. [34] |
В последнем случае реакция состоит из быстро затормаживающейся макроскопической стадии, в которой при участии пропана, О2 и НВг образуется относительно устойчивый промежуточный продукт ( строение его не установлено), играющий роль инициатора цепного окисления пропана в ацетон во второй макроскопической стадии. [35]
 |
Скорость мономолекулярного распада перекиси водорода ( 1 и органических гидроперекисей ( 2 при температуре 115. [36] |
С появлением максимумов по перекисным соединениям связано начало следующей макроскопической стадии процесса - стадии образования нового продукта - уксусной кислоты. Накопление ее, так же, как и накопление других продуктов реакции, носит автоускоренный характер, что свидетельствует о наличии цепного механизма этой реакции. Количество уксусной кислоты возрастает по мере расходования перекисных соединений. Одновременно наблюдается и ускорение накопления ацетона. [37]
Основываясь на принципах цепной теории и гипотезе о макроскопических стадиях, Эмануэль совместно с Денисовым [ 144J подробно осветил вопросы о механизме действия ингибиторов в реакциях жидкофазного окисления. Главные положения теории-действия ингибиторов сводятся к следующему. [38]
Особенно четко стадийный механизм процесса ( разделяющиеся во времени макроскопические стадии) был показан в наших работах по изучению катализированных процессов окисления углеводородов в газовой фазе [8], а также в работах В. К. Цысковского [9], Б. К. Зейналова [10] и наших [11, 12] для катализированного окисления жидких углеводородов. [39]
Превращение комплекса Михаэлиса в конечные продукты осуществляется в две макроскопические стадии. [40]
Наблюдаемое явление резкого изменения режима процесса свидетельствует о наличии двух макроскопических стадий, протекающих по раз-лпчному механизму; причем первая стадия подготавливает условия для развития второй макростадии процесса аналогично тому, как это было установлено одним из нас [13] для ряда химических реакций. [42]
Данные по распаду гидроперекисей свидетельствуют в пользу того, что макроскопическими стадиями, следующими непосредственно за образованием гидроперекисей, являются образования спиртов и карбонильных соединений. [43]
Кинетика процесса окисления изопропилового спирта свидетельствует о наличии в процессе ряда параллельных и последовательных макроскопических стадий и автокаталитическом характере этого процесса. [44]
Кинетика процесса окисления нзопронилового спирта свидетельствует о наличии в процессе ряда параллельных и последовательных макроскопических стадий и автокаталитическом характере этого процесса. [45]
Страницы: 1 2 3 4
