Степень - диссоциация - кислота
Cтраница 3
Значение Е зависит от степени диссоциации кислоты ( или основания), но константа диссоциации этой кислоты ( или основания) в данном растворителе может в значительной степени отличаться от / Сндп слабой кислоты ( или слабого основания), для смеси которой с ее солыо в буферном растворе, содержащем равные концентрации кислоты ( основания) и соли, применимо уравнение ( 37), поэтому для данного случая ( когда рН ф р / С) уравнение ( 37) оказывается Несостоятельным. [31]
Величина рН зависит от степени диссоциации кислоты или щелочи и их содержания в растворе. [32]
Отмеченная нами связь между степенью диссоциации кислот и их химической активностью отнюдь неслучайна. [33]
Величина теплоты нейтрализации зависит от степени диссоциации взаимодейстиующих кислот и оснований и от характера ядра органического соединения и имеющихся заместителей. [34]
Особенно велика разница в значениях степени диссоциации кислот. [35]
Здесь мы будем говорить только о степени диссоциации кислот и оснований в водных растворах и обсудим влияние лишь одной переменной - природы растворяемого вещества. [36]
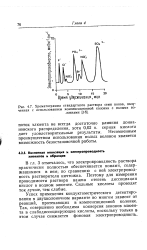 |
Хроматограмма стандартного раствора семи ионов, полученная с использованием компенсационной колонки с полыми волокнами. [37] |
Поэтому для измерения проводимости раствора важна степень диссоциации кислот в водном элюенте. Сильные кислоты проводят ток лучше, чем слабые. [38]
Видим, что прибавление соли понизило степень диссоциации кислоты в 20 раз. [39]
Выражение ( 22) позволяет вычислить степень диссоциации кислоты, если известны ее концентрация и константа диссоциации. [40]
Результаты опытов показали, что влияние степени диссоциации кислот на величину сорбции имеет место лишь на сильнонабухающих ионитах при малых скоростях потока. [41]
 |
Сорбция растворов кислот в пленках полимеров. [42] |
Коэффициент диффузии в твердых полимерах зависит также от степени диссоциации кислот в силу разной подвижности различных ионов и недиссоциированных молекул. [43]
Соотношение между активной и общей кислотностью зависит только от степени диссоциации кислоты в данном растворе. Чем меньше степень диссоциации, тем меньшую долю общей кислотности составляет активная кислотность. Наоборот, при высокой степени диссоциации разница между ними незначительна, и в пределе, когда степень диссоциации равна единице ( а1), активная кислотность равна общей. Это имеет место в разбавленных растворах сильных кислот. [44]
Соотношение между активной и общей кислотностью зависит только от степени диссоциации кислоты в данном растворе. Чем меньше степень диссоциации, тем меньшую долю общей кислотности составляет активная кислотность. Наоборот, при высокой степени диссоциации разница между ними незначительна и в пределе, когда степень диссоциации равна единице ( а 1), активная кислотность равна общей. Это имеет место в разбавленных растворах сильных кислот. [45]
Страницы: 1 2 3 4