Степень - достижение - равновесие
Cтраница 3
Для расчета барботажных поглотительных колонн этот метод дает результаты, хорошо согласующиеся с практическими. Точность результатов повышается при введении коэффициента, характеризующего степень достижения равновесия между газами и кислотой; коэффициент определяется практически. Так, для стандартной колонны диаметром 1 7 м с 26 тарелками и 36 барботажными колпачками, рассчитанной на поглощение окислов азота под давлением 7 ат, введен поправочный коэффициент С, который при нагрузке 10 6 т НМО3 в сутки равен 0 45 для 57 % - ной кислоты и 0 39 для 16 % - ной кислоты. [31]
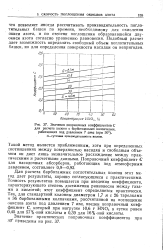 |
Значения поправочных коэффициентов С. [32] |
Для расчета барботажных поглотительных колонн этот метод дает результаты, хорошо согласующиеся с практическими. Точность результатов повышается при введении коэффициента, характеризующего степень достижения равновесия между газами и кислотой; этот коэффициент определяется практически. Та К, для стандартной колонны диаметром 1 7 м с 26 тарелками и 36 барботажными колпачками, рассчитанной на поглощение окислов азота под давлением 7 ата, введен поправочный коэффициент С, который при нагрузке 10 6 т HNO3 в сутки равен 0 46 для 57 % - ной кислоты и 0 39 для 16 % - ной кислоты. [33]
Простые обратимые реакции идут с образованием одного продукта. Выход этого продукта зависит от положения равновесия и от степени достижения равновесия за время пребывания реакционной смеси в зоне реакции. Объектами регулирования здесь являются положение равновесия и скорость реакции. [34]
 |
Принципиальная схема двухтемпературного процесса. [35] |
В работе Розена [6, 7] подробно рассмотрен расчет такого каскада. Степень извлечения зависит от температуры горячей и холодной колонн и степени достижения равновесия на концах колонн. [36]
Для расчета барботажных поглотительных колонн этот метод дает хорошо согласующиеся с практикой результаты. Точность результатов повышается при введении в расчет коэфициента, характеризующего степень достижения равновесия между газами и кислотой. Этот коэфициент определяется практически. Так, для стандартной колонны диаметром 1 7 м с 26 тарелками и 36 барботажными колпачками, рассчитанной на поглощение окислов азота под давлением 7 ата, введен поправочный коэфициент F, который при нагрузке в 10 6 г HNO3 в сутки равен 0 45 для 57 % - ной кислоты и 0 39 для 16 % - ной кислоты. [37]
Если две или более фаз находятся в тесном контакте, возникает потенциал, способствующий самопроизвольному переходу вещества через границы фаз, и система стремится к состоянию равновесия. Состояние равновесия характеризуется комплексом условий, к которым приближается неравновесная система как к пределу; в большинстве случаев степень достижения равновесия настолько велика, что различие между реальным состоянием и равновесным находится в пределах ошибки опыта. Знание условий равновесия имеет первостепенное значение в таких технических процессах, как абсорбция, адсорбция, экстракция, дистилляция, испарение, высушивание и кристаллизация. Критерий для определения условий равновесия был разобран в гл. Из всех возможных комбинаций фаз и веществ ниже будет рассмотрена только двухфазная система неэлектролитов, в котором одна из фаз - пар. [38]
Это связано с тем, что на практике определяющее значение, кроме остаточного давления, имеет скорость и степень достижения равновесия массооб-мена этиленгликоля между жидкой и паровой фазой, что в конце концов оказывает значительное влияние и на глубину прохождения побочных процессов. Однако данные по уравнению Гриля - Форстера болев соответствуют практически получаемым, чем по уравнению с поправками Дитце. [39]
 |
Хлорирование борного ангидрида в присутствии твердого восстановителя. [40] |
Если процесс идет только - до образования СО, реакция эндотер-мична. Хлорирование в присутствии твердого восстановителя идет по уравнениям (6.8) и (6.9), причем их соотношение обусловливается в определенной мере степенью достижения равновесия реакции Будуара. [41]
В силу стохастического характера явлений массопереноса достижение равновесного состояния подчинено вероятностным законам распределения энергии и массы в пространстве и во времени. Если принять во внимание, что время контакта фаз пропорционально межфазной поверхности, то можно сделать вывод о том, что степень достижения равновесия на ступени разделения определяется гидродинамической обстановкой и в конечном счете должна учитываться при определении эффективности. [42]
В силу стохастического характера явлений массопереноса достижение равновесного состояния подчинено вероятностным законам распределения энергии и массы в пространстве и Времени. К наиболее существенным причинам неравновесности массообмена в промышленных условиях можно отнести: неравномерность распределения частиц потока по времени пребывания; обратный заброс фаз в результате механического уноса; недостаточные в) ремя контакта фаз или величина межфазной поверхности контакта. Степень достижения равновесия на ступени разделения определяется гидродинамикой потоков жидкости и пара, их взаимодействием, а следовательно, временем пребывания в аппарате. [43]
В силу стохастического характера явлений массопереноса достижение равновесного состояния подчинено вероятностным законам распределения энергии и массы в пространстве и по времени. Степень достижения равновесия на ступени разделения определяется гидродинамикой потоков жидкости и пара, их взаимодействием, а следовательно, временем пребывания в аппарате. [44]
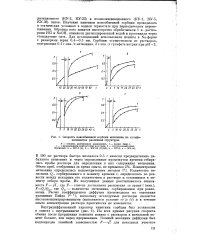 |
Скорость ионообменной сорбции метионина на сульфо-катионитах различной структуры. [45] |
Страницы: 1 2 3 4