Степень - достижение - равновесие
Cтраница 4
В 100 мл раствора быстро вносилось 0.5 г навески предварительно набухшего катионита и через определенные промежутки времени отбирались пробы раствора для определения в них содержания метионина. Из полученных данных рассчитывалась зависимость F - jt, где F - - степень достижения равновесия за время t ( мин. [46]
Непосредственное взаимодействие между окисью углерода и водяным паром имеет место лишь при температуре 1000 С и выше. При более низких температурах реакция идет только в присутствии катализаторов. В зависимости от активности катализатора процесс может быть осуществлен при различной температуре и с различной скоростью, что сказывается на степени достижения равновесия, содержании окиси углерода после реакции и на производительности катализатора. [47]
Практически тип кинетики устанавливают, выявляя зависимость скорости установления равновесия от тех или иных факторов эксперимента. Если равновесие устанавливается достаточно быстро, независимо от величины зерна ионита, то имеет место химическая кинетика. Гелевую и пленочную кинетику легко различить, используя так называемый метод прерывания: ионит отделяют от раствора, находящегося с ним в контакте, фазы выдерживают порознь некоторое время, а потом опять приводят в контакт. Если степень достижения равновесия системы в результате прерывания контакта фаз возросла по сравнению с системой, где при прочих равных условиях контакт не прерывался ( время контакта фаз в обоих опытах одинаково), делают вывод о геле-вой кинетике. Поскольку увеличение времени на такое выравнивание способствовало достижению равновесия, очевидно, что лимитирующим процессом в системе была внутренняя диффузия. При пленочной кинетике прерывание контакта фаз не изменяет скорость достижения равновесия. [48]
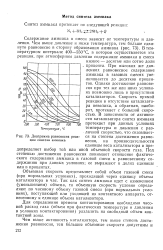 |
Диаграмма равновесия реакции синтеза аммиака. [49] |
При высоких же давлениях равновесное содержание аммиака в газовых смесях увеличивается до десятков процентов. Однако достижение равновесия при тех же или иных условиях возможно лишь в присутствии катализаторов. Скорость прямой реакции в отсутствие катализатора невелика, а обратная, наоборот, протекает с большой скоро стью. В зависимости от активности катализатора синтез аммиака протекает при данных условиях температуры и давления с различной скоростью, что сказывается на степени достижения равновесия, на производительности единицы веса катализатора и предопределяет выбор той или иной объемной скорости газа. Под степенью достижения равновесия понимают отношение фактического содержания аммиака в газовой смеси к равновесному содержанию при данных условиях; ее выражают в долях единицы или в процентах. [50]
При высоких же давлениях равновесное содержание аммиака в газовых смесях увеличивается до десятков процентов. Однако достижение равновесия при тех же или иных условиях возможно лишь в присутствии катализаторов. Скорость прямой реакции в отсутствие катализатора невелика, а обратная, наоборот, протекает с большой скоро стью. В зависимости от активности катализатора синтез аммиака протекает при данных условиях температуры и давления с различной скоростью, что сказывается на степени достижения равновесия, на производительности единицы веса катализатора и предопределяет выбор той или иной объемной скорости газа. Под степенью достижения равновесия понимают отношение фактического содержания аммиака в газовой смеси к равновесному содержанию при данных условиях; ее выражают в долях единицы или в процентах. [51]
Повышение давления до 1 at уменьшает объем реакционного пространства абсорберов в 20 - 25 раз. Обогащение кислородом при NO: Оа 1: 1 6, и 17 % азота в газе ( 93 % - ный кислород как источник О2) уменьшает объем в 3 раза. Пастонези сообщает, что пущен з-д, на к-ром окисление NO ведут в присутствии силика-геля как катализатора. Повышение давления при абсорбции помимо снижения капиталовложений позволяет получать более концентрированную А. I) и ( IV) необходимое время соприкосновения чрезвычайно увеличивается, и вместо секунд требуются часы. Степень достижения равновесия в реакции ( IV) уменьшается с увеличением концентрации к-ты, уменьшением парциального давления окислов азота и увеличением скорости газового потока. [52]
Страницы: 1 2 3 4