Степень - ионность
Cтраница 1
Степень ионности или ковалентнос-ти связи характеризуется электронной плотностью. [1]
 |
Взаимосвязь между точкой плавления а и характером связи. [2] |
Степень ионности можно оценить несколькими методами, но, вероятно, самым прямым из них является электронная спектроскопия соединений данного элемента. Интервалы между электронными энергетическими уровнями, безусловно, зависят от межатомных взаимодействий, и изменения расположения этих уровней вызовут изменения в спектре. Невзаимодействующие ионы, по-видимому, будут иметь наиболее простые спектры, поскольку они обладают наивысшей симметрией и наименьшими энергиями взаимодействия с соседними ионами. Для ковалентно связанных атомов можно ожидать, что электронные спектры будут сильно зависеть от природы атомов, образующих ковалент-ные связи. Это и наблюдается в действительности. [3]
Степень ионности ( или процент ионности) химической связи определяется как отношение эффективного заряда к заряду электрона. [4]
Степень ионности можно оценить несколькими методами, но, вероятно, самым прямым из них является электронная спектроскопия соединений данного элемента. Интервалы между электронными энергетическими уровнями, безусловно, зависят от межатомных взаимодействий, и изменения расположения этих уровней вызовут изменения в спектре. Невзаимодействующие попы, по-видимому, будут иметь наиболее простые спектры, поскольку они обладают наивысшей симметрией и наименьшими энергиями взаимодействия с соседними ионами. Для ковалентно связанных атомов можно ожидать, что электронные спектры будут сильно зависеть от природы атомов, образующих ковалент-ные связи. Это и наблюдается в действительности. [5]
Степень ионности остается все же неопределенной. [6]
Степень ионности межатомной связи можно определить по величине эффективного заряда атомов, которая отражает распределение электронной плотности. Величину эффективного заряда, в свою очередь, определяют из рентгеновских данных ( например, для атома кремния в ряде его соединений - путем измерения смещения / Саь2 линий), по величине теплоты сублимации, методом аннигиляции позитронов. Этот последний метод интересен не только сам по себе. [7]
Степень ионности сульфонатов двухвалентных металлов значительно выше, чем у одновалентных, - у последних ниже диэлектрическая проницаемость и выше ККМ. Наоборот, растворимость в воде и водоудерживающие свойства у сульфонатов одновалентных металлов значительно выше, чем у двухвалентных. [8]
 |
Свойства минералов. [9] |
Степенью ионности называют долю ионного характера связи. Ионную связь можно рассматривать как предельную полярную химическую связь, для которой эффективный заряд атома близок к единице. [10]
Степенью ионности соединения: обычно в ионных соединениях, где изменения потенциала особенно ощутимы, подвижность низка; с другой стороны, в кристаллах с ковалентной связью ( где отсутствует чередование положительных и отрицательных ионов) подвижность носителей значительно выше. Сравнение ряда изоморфных кристаллов, таких как, например, PbS, PbSe, PbTe, ясно показывает, как увеличивается подвижность при переходе от ионной к ковалентной связи. [11]
Степенью ионности соединения: обычно в ионных соединениях, где изменения потенциала особенно ощутимы, подвижность низка; с другой стороны, в кристаллах с ковалентной связью ( где отсутствует чередование положительных и отрицательных ионов) подвижность носителей значительно выше. Сравнение ряда изоморфных кристаллов, таких как, например, PbS, PbSe, РЬТе, ясно показывает, как увеличивается подвижность при переходе от ионной к ковалентной связи. [12]
Причем степень ионности переходного состояния выражается по-разному в зависимости от исходного углеводорода, галогена и катализатора. [13]
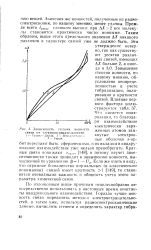 |
Зависимость степени ионное ги. [14] |
Завышение степени ионности, по нашему мнению, обусловлено неопределенностью в учете гибридизации, поляризации и кратности связей. [15]
Страницы: 1 2 3 4