Степень - ионность
Cтраница 2
Влияние степени ионности на величины показателей преломления кристаллов с переходным ( ионно-ко-валентным) типом связи было рассмотрено в XII главе, § 8, стр. [16]
Чему равна степень ионности каждой из этих молекул в процентном выражении. Данные о дипольных моментах указанных молекул следует найти в справочниках. [17]
Независимо от степени ионности ковалентные связи образуются только при сближении двух атомов, у каждого из которых имеется орбиталь только с одним электроном. Химики называют такую орби-таль наполовину заполненной, так как на каждой орбитали, будь то атомная или молекулярная орбиталь, могут разместиться два электрона. [18]
 |
Ионность связи в гидратированных молекулах. [19] |
Сначала определим степени ионности соответствующих электростатических связей, для чего подставим в урав нение ( стр. Полученные таким образом величины выписаны в табл. 59 во вторых строчках. [20]
 |
Ионности связей по радиоспектроскопическим данным. [21] |
Табулированные значения степеней ионности представлены в графическом виде на рис. 4 в зависимости от разницы электроотрицательностей. Однако по абсолютным величинам данные табл. 37 значительно превышают значения Полинга. [22]
Различие между степенью ионности этих двух типов связей олово - галоген составляет 12 5 % для хлоридов и 7 5 % для бромидов. Вследствие координации до-норных растворителей разница между этими двумя типами связей уменьшается [287, 288], что вызывает уменьшение градиента электрического поля и, следовательно, квадрупольного расщепления. [23]
Пйлярность, или степень ионности, связи сказывается не только на физических свойствах соединения в соответствии с общеизвестными характеристиками ионных и ковалентных соединений, но также заметно влияет на химическую активность соединения. [24]
Зависимость Д5 от степени ионности образующихся в твердом растворе химических связей является более сложной. [25]
По мере увеличения степени ионности ковалентной связи ширина запрещенной зоны постепенно увеличивается. [26]
К иногда называют степенью ионности. [27]
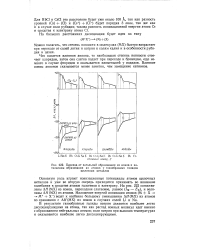 |
Переход от энтальпий образования из ионов к энтальпиям образования из атомов у газообразных галидов щелочных металлов. [28] |
Можно полагать, что степень ионности в молекулах ( MX) быстро возрастает при переходе от солей лития и натрия к солям калия и в особенности рубидия и цезия. [29]
При небольших удлинениях ОН-связи степень ионности ее в соответствии с указанным выше, сначала несколько увеличивается, а затем падает. В результате этого диссоциация протекает гомолитически. При образовании комплекса с водородной связью происходит взаимная поляризация молекулы основания и ОН-группы, вследствие чего степень ее ионности увеличивается. Еще больше растет степень ионности ОН-связи по мере ее удлинения. Поэтому диссоциация, начинаясь как гемолитическая, заканчивается как гетеролитическая. Эта способность ОН-групп изменять характер диссоциации в присутствии сильных акцепторов протона и является мерой их реакционной способности в реакциях кислотно-основного типа. [30]
Страницы: 1 2 3 4