Степень - ионность
Cтраница 3
Близкими к 100 % степенями ионности обладают связи между самыми электроположительными и самыми электроотрицательными элементами. [31]
Еков, которое определяется степенью ионности соединения, величина поляризации зависит от суммарного порядкового номера. С увеличением этой суммы поляризация растет. [32]
 |
Эффективные заряды атомов в некоторых соединениях. [33] |
Долю частично ионного характера ( степень ионности или ионность) ковалентной связи можно оценить, если известны элекгроотрицательности взаимодействующих атомов А и В. Заметим, что при анализе характера связи обычно принято рассматривать не сами электроотрицательности, а разность электроотрицательностеи взаимодействующих атомов. [34]
 |
Водородно-хлорный элемент. [35] |
Расхождение значительное, так как степень ионности в кристаллах А1С13 невелика и сохраняются ковалентные связи. [36]
Как определяется и что показывает степень ионности химической связи. [37]
В табл. 45 сопоставлены значения степеней ионности, определенные экспериментально ( среднее из табл. 41 и 43) - первые строчки, и вычисленные по правилу Полинга - вторые строчки; относительно значений, приведенных в последних строчках, будет сказано ниже. [38]
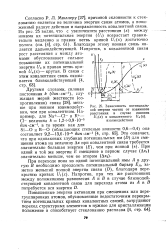 |
Зависимость потенциальной энергии частиц от взаимного расстояния в случае ионного Ui ( x и ковалентного Ua ( x взаимодействия. [39] |
О и В-О ( обладающих степенью ионности 0 6 - 0 4) она составляет 9 2 - 13 6 - 10 - 5 дин-смг 1 [ 4, стр. [40]
Расхождения значительно больше, так как степень ионности в кристаллах А1С1з невелика и существуют ковалентные связи. В реально работающих гальванических элементах ( / 0) получаемая работа меньше, так как за счет явлений поляризации ( которые будут рассмотрены далее) разность потенциалов меньше. [41]
Очевидно, что в случае а степень ионности в молекуле будет мала, а в случае б - велика. [42]
Суш ествуют разные уравнения, связывающие степень ионности с электроотрицательностью атомов или атомных групп, входящих в молекулу. [43]
В случае молекул типа АВ3 расчет степени ионности еще более сложен. Исходя из того, что радикалы типа АВ известны, а типа АВ2 практически не изучены, мы считаем целесообразным вычислять / следующим образом. Вначале находим / первой связи по & Х Х - Ав, затем предполагаем, что остальные атомы присоединились все сразу. [44]
Энергия связывающего состояния увеличивается с ростом степени ионности, однако она является лишь частью полной энергии связи... В ковалентных-кристаллах на это важное различие часто не обращают внимания, что приводит к путанице. В гомеополярных полупроводниках полная энергия связи в расчете fta одну связь сравнима по величине с энергией ковалентной связи 1 / 2 и имеет такую же зависимость от степени металличнос ти. [45]
Страницы: 1 2 3 4