Степень - окисление - центральный атом
Cтраница 3
Такая закономерность - усиление кислотных свойств гидроокиси с возрастанием степени окисления центрального атома - характерна не только для хлора, но и для других элементов. [31]
Если центральный атом кислоты является элементом I-VI групп, то степень окисления центрального атома, соответствующую номеру группы, обозначают суффиксом ат, который добавляют к корню латинского названия центрального атома кислоты, затем называют металл: КзА1О3 - ортоалюминат калия, КРО3 - мета-фосфат калия, BaSeO4 - селенат бария. [32]
Если центральный атом кислоты является элементом I-VI групп, то степень окисления центрального атома, соответствующую номеру группы, обозначают суффиксом ат, который добавляют к корню латинского названия центрального атома кислоты, затем называют металл: КзА1О3 - - ортоалюминат калия, КРОз - мета-фосфат калия, BaSe04 - селенат бария. [33]
К классическим комплексным соединениям относятся соединения, в которых формально превышается степень окисления центрального атома. Большая часть принципов построения их названий была рассмотрена выше. Основные положения можно кратко сформулировать следующим образом: комплекс может быть катионным, нейтральным или анионным. В англо-американской литературе названия лигандов перечисляются по алфавиту. [34]
Поскольку обе кислоты содержат одинаковое число групп ОН, метод оценки относительной кислотности по степени окисления центрального атома тоже приводит к правильному предсказанию. [35]
В орто-производных количество атомов кислорода в молекуле равно количеству атомов водорода и численно равно степени окисления центрального атома. Исключение составляют кислоты элементов V группы общей формулы НсЭ04, которые считаются ортогидроксндами и называются, например, ортофосфорнон Н3РО4, ортомышьяко - ЕОЙ H3As04 кислотами. [36]
Существует еще одно правило предсказания сравнительной силы кислородсодержащих кислот, основанное на учете отношения степени окисления центрального атома к числу связанных с ним атомов: чем больше это отношение, тем сильнее соответствующая кислота. [37]
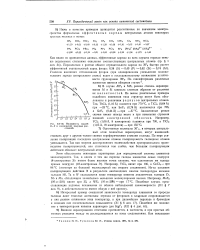 |
Полярность связей Э - F и сокращение ядерных расстояний. [38] |
Как видно из приведенных данных, эффективные заряды во всех случаях гораздо меньше задаваемых степенями окисления соответствующих центральных атомов ( ср. [39]
Трифенилфосфин и родственные ему соединения, как известно, также обладают способностью стабилизировать интермедиаты с низкой степенью окисления центрального атома. [40]
Особый интерес для химии комплексных соединений этот метод может представлять потому, что он наглядно и количественно может показать влияние степени окисления центрального атома на прочность связи его с аддендами. [41]
 |
Орбитали dza ( о, dxi v2 ( б, и d ( в в октаэдрическом поле лигандов ( лиганды условно обозначены в виде шариков. [42] |
Взаимное расположение лигандов с близкими энергиями расщепления может несколько изменяться при переходе к другому центральному атому или даже при изменении степени окисления центрального атома. [43]
В случае неэлектролитов ( комплексообразователь и лиганды образуют не внутреннюю, а единственную комплексную сферу с нулевым зарядом) вместе с ли-гандами степень окисления центрального атома не приводят, так как она однозначно определяется, исходя из электронейтральности комплекса. [44]
 |
Константы кислотности Ка кислородсодержащих кислот и электроотрицательность их центрального атома Y. [45] |
Страницы: 1 2 3 4