Степень - окисление - центральный атом
Cтраница 4
В ряду кислот с одинаковым центральным атомом Y, но с разным числом присоединенных к нему групп сила кислоты увеличивается с возрастанием степени окисления центрального атома. [46]
Однако здесь, в отличие от примеров с непереходными элементами, доступность таких соединений обусловливается, главным образом, изменениями координационного числа и степени окисления центрального атома. Ввиду этого, возможно, покажется удивительным, что в литературе не встретились другие примеры; можно было бы ожидать образование комплексов металлов группы VIIIA и VIIIB с координационным числом пять или шесть. Следует отметить, что идентификация таких комплексов требует особого внимания. Недавно получены фталоцианиновые производные рутения, осмия и иридия как аддукты с фталонитрилом. Делается предположение [82], что фталонитрил удивительно прочно связывается, если он выступает в роли лиганда. [47]
Аналогичный эффект наблюдается, если наличие внешнего реагента приводит к образованию неустойчивой системы металл - лиганд, которая в свою очередь способствует изменению степени окисления центрального атома металла. Образование системы такого типа осуществляется в окислительно-восстановительных реакциях с мостиковыми лигандами. Эти реакции будут описаны ниже ( стр. [48]
Сила кислот существенно возрастает в ряду НС1 О - НСГ 04 ( НСЮ - очень слабая кислота, НСЮ4 - самая сильная кислота из всех известных) Такая закономерность - усиление кислотных свойств с возрастанием степени окисления центрального атома характерна не только для хлора, но и для других элементов. Так, константа кислотной диссснданиви НГ О в 250 раз меньше таковой дляНСТ О. [49]
С увеличением степени окисления центрального атома сила кислот обычно возрастает. [50]
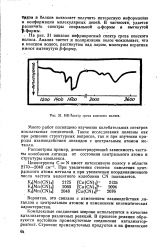 |
ИК - пек р среза конского волоса. [51] |
Цианогруппа С N имеет интенсивную полосу в области 2170 - 2040 см-1. При увеличении степени окисления центрального атома металла и при увеличении координационного числа частота валентного колебания CN понижается. [52]
 |
Кривая потенций метрического титрования для окислительно-восстановительной реакции. [53] |
Следует обратить внимание на то обстоятельство, что при рассмотрении оксианионов речь идет об электроотрицательности атома, входящего в состав молекулы или радикала, а не находящегося в свободном состоянии. По мере возрастания степени окисления центрального атома его электроотрицательность должна увеличиваться, так как при этом возрастает положительный заряд и уменьшается размер атома. [54]
 |
Растворимость хлоридов при 20 С, г / 100 г Н20. [55] |
Гидроксиды кислотного типа типично неметаллических элементов обычно хорошо растворимы. По мере снижения степени окисления центральных атомов анионов кислотные свойства гидроксидов уменьшаются и растворимость снижается. Лишь высшие гидроксиды металлов В-подгрупп VI и VII групп - хромовые ( Н2СгО4 и НаСг2О) и марганцовая ( НМпО4) кислоты-характеризуются большой растворимостью. [56]
Страницы: 1 2 3 4