Степень - полярность - связь
Cтраница 2
 |
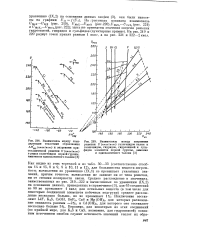
График для определения, , Лг п нгч ырг HI. [16] |
Падение р в этом ряду объясняется тем, что уменьшение различия в электроотрицательностях уменьшает степень полярности связи. [17]
 |
Влияние кратности связи на расстояния ( в А между ядрами атомов.| Расположение атомов в молекулах. а - ССЦ ( правильный тетраэдр и б - SFg ( правильный октаэдр. [18] |
Так, в частности, расстояние между атомами, связанными полярной связью, зависит от степени полярности связи. [19]
В этом случае оно определяется характером, химической связи между ними, степенью различия в их относительной электроотрицательности и, следовательно, степенью полярности связи. Например, если судить по суммарным формулам, то в молекуле метана ( СН4) и в молекуле метилового спирта ( СН4О) все четыре атома водорода должны обладать одинаковыми свойствами. Но, как будет показано дальше, в метиловом спирте один из атомов водорода способен замещаться щелочным металлом, тогда как в метане атомы водорода такой способности не проявляют. [20]
Как видно из этих чертежей и из табл. 30 - 33 ( соответственно столбцы 14 и 15, 8 и 9, 9 и 10, 11 и 12), для большинства веществ погрешность вычисления по уравнению ( IX, 1) не превышает указанных значений, причем точность вычисления не зависит ни от типа решетки, ни от степени полярности связи. [22]
 |
Поляризация ионов в молекуле и результирующий дипольный момент. [23] |
Степень полярности связи наиболее непосредственно характеризуется диполь-ным моментом, часто для этого используется также концепция электроотрицательности. Полинг назвал электроотрицательностью атома ( ЭО) способность его в молекуле притягивать на себя электрон. Полярность молекулы определяется разностью электроотрицательно-стей атомов ( ДЭО), чем она выше, тем полярнее связь. Поэтому мерок электроотрицательности может служить сумма ПИ и СЭ. [24]
 |
Модель молекулы димерного триметилалюминия. [25] |
Если у а-углеродного атома в алюминийалкиле остается атом водорода ( например, у вторичных алкильных радикалов), ассоциация молекул протекает незначительно. Степень полярности связи зависит, как обычно, от соотношения энергетических уровней соответствующих электронных орбиталей. [26]
 |
Поляризация ионов в молекуле. [27] |
Степень полярности связи наиболее непосредственно характеризуется диполь-ным моментом, часто для этого используется также концепция электроотрицательности. Полинг назвал электроотрицательностью атома ( ЭО) способность его в молекуле притягивать на себя электрон. Полярность молекулы определяется разностью электроотрицательно-стей атомов ( ДЭО), чем она выше, тем полярнее связь. Поэтому мерой электроотрицательности может служить сумма ПИ и СЭ. [28]
Какие ковалентные связи называют неполярными и полярными. Чем определяется степень полярности связи. [29]
Сера окисляет целый ряд простых веществ, давая сульфиды. В зависимости от степени полярности связи образуются либо ионные, либо полярные молекулярные ( S4N4) вещества, либо вещества промежуточного типа. Последний случай реализуется наиболее часто, например полимерные ковалентные соединения SiSz, 80283 и BisSs, а также нестехиометрические фазы многих сульфидов металлов, обладающие сходством с металлическими веществами. [30]
Страницы: 1 2 3 4