Степень - полярность - связь
Cтраница 3
В меньшей степени способность связываться с другими молекулами сохраняет водородный атом, связанный с атомами азота или хлора. Впрочем, как мы видели в § 20, степень полярности связи зависит не только от вида атома, с которым непосредственно связан данный атом, но также и от того, с какими атомами связаны эти атомы другими валентностями. [31]
В меньшей степени способность связываться с другими молекулами сохраняет водородный атом, связанный с атомами азота или хлора. Впрочем, как мы видели в § 20, степень полярности связи зависит не только от вида атома, с которым непосредственно связан данный атом, но также и от того, с какими атомами связаны эти атомы другими валентностями. Так, водородный атом, связанный с кислородом или азотом, будет более способен к образованию водородной связи, если атомы кислорода или азота другой своей валентностью связаны с более электроотрицательным элементом. [32]
В меньшей степени способность связываться с другими молекулами сохраняет водородный атом, связанный с атомами азота или хлора. Впрочем, как мы видели в § 16, степень полярности связи зависит не только от вида атома, с которым непосредственно связан данный атом, но также и от того, с какими атомами связаны эти атомы другими валентностями. Так, водородный атом, связанный с кислородом или азотом, будет более способен к образованию водородной связи, если атомы кислорода или азота другой своей валентностью связаны с более электроотрицательным элементом. [33]
В меньшей степени способность связываться с другими молекулами сохраняет водородный атом, связанный с атомами азота или хлора. Впрочем, как мы видели в § 20, степень полярности связи зависит не только от вида атома, с которым непосредственно связан данный атом, но также и от того, с какими атомами связаны эти атомы другими валентностями. Так, водородный атом, связанный с кислородом или азотом, будет более способен к образованию водородной связи, если атомы кислорода или азота другой своей валентностью связаны с более электроотрицательным элементом. [34]
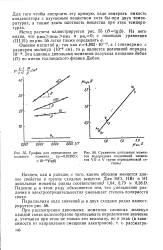 |
График для определения ди - [ IMAGE ] Сравнение дипольных момен. [35] |
Начнем, как и раньше, с того, каким образом меняется данное свойство в группе сходных веществ. Падение л в этом ряду объясняется тем, что уменьшение различия в электроотрицательностях уменьшает степень полярности связи. [36]
Интерес к изучению азотсодержащих систем [603] объясняется тем, что атом азота в составе различных соединений может обусловливать как кислотные, так и основные свойства. Очевидно, что определяющими факторами, кроме стерического, в данном случае служит состояние неподеленной пары электронов и степень полярности связей азота. Прочность водородной связи с участием группы - NH2 и способность азота к комплексообразованию представляют интерес и с точки зрения установления соответствия между прочностью водородной связи и строением соединений. [37]
В соответствии с изменением химической природы элемента закономерно изменяются и химические свойства соединений, в частности их основно-кислотная активность. Так, в случае оксидов в ряду Li20 - BeO - B2O3 - CO2 - N2O5 по мере уменьшения степени полярности связи ( уменьшения отрицательного эффективного заряда атома кислорода 8) ослабляются основные и нарастают кислотные свойства: Li2O - сильно основной оксид, ВеО - амфотерный, а В2Оз, СО2 и N2O5 - кислотные. [38]
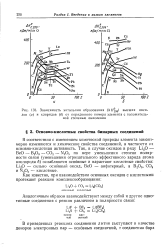 |
Зависимость энтальпии образования ( ДЯ дд высших оксидов ( а и хлоридов ( б от порядкового номера элемента с положительной степенью окисления. [39] |
В соответствии с изменением химической природы элемента закономерно изменяются и химические свойства соединений, в частности их основно-кислотная активность. Так, в случае оксидов в ряду Li2O - ВеО - В2О3 - СО2 - N2O5 по мере уменьшения степени полярности связи ( уменьшения отрицательного эффективного заряда атома кислорода 6) ослабляются основные и нарастают кислотные свойства: Li2O - сильно основный оксид, ВеО - амфотерный, а В2О3, СО2 и N2O5 - кислотные. [40]
В соответствии с изменением химической природы элемента закономерно изменяются и химические свойства соединений, в частности их основно-кислотная активность. Так, в случае оксидов в ряду Li2O - ВеО - В2О3 - СО2 - N2O6 по мере уменьшения степени полярности связи ( уменьшения отрицательного эффективного заряда атома кислорода 6) ослабляются основные и нарастают кислотные свойства: Li2O - сильно основный оксид, ВеО - амфотерный, а В2О3, СО2 и N2O5 - кислотные. [41]
 |
Зависимость энтальпии образования ( AW gg высших оксидов ( а и хлоридов ( б от порядкового номера элемента с положительной степенью окисления. [42] |
В соответствии с изменением химической природы элемента закономерно изменяются и химические свойства соединений, в частности их основно-кислотная активность. Так, в случае оксидов в ряду Li2O - ВеО - В2О3 - СО2 - N2O5 по мере уменьшения степени полярности связи ( уменьшения отрицательного эффективного заряда атома кислорода б) ослабляются основные и нарастают кислотные свойства: Li2O - сильно основный оксид, ВеО - амфотерный, а В2О3, СО2 и N. [43]
В соответствии с изменением химической природы элементов закономерно изменяются и химические свойства соединений. Так, в случае оксидов в ряду Li2O - ВеО - В2О3 - - СО2 - N2O5 по мере уменьшения степени полярности связи ослабляются основные и нарастают кислотные свойства: Li2O - основной оксид, ВеО - амфотерный, а В2О3, СО2 и N2O5 - кислотные. [44]
Взаимное влияние в молекулах органических веществ проявляют прежде всего атомы, непосредственно связанные друг с другом. В этом случае оно определяется характером химической связи между ними, степенью различия в их относительной электроотрицательности и, следовательно, степенью полярности связи. [45]
Страницы: 1 2 3 4