Степень - алкилирование
Cтраница 3
Количество катализатора в пределах 0 2 - 0 5 моля на 1 моль оле-фина не оказывает заметного влияния на выход алкилата. Однако существует некоторый минимум для BFs НзР04, ниже которого степень алкилирования сильно падает. [31]
Количество катализатора в пределах 0 2 - 0 5 моля на 1 моль оле-фина не оказывает заметного влияния на выход алкилата. Однако существует некоторый минимум для BF3 - H3P04, ниже которого степень алкилирования сильно падает. [32]
Попытки метилировать органические соединения метиловым спиртом, йодистым метилом и метилацетатом оказались также безуспешными [122], несмотря на то, что аналогичные реакции в присутствии хлористого алюминия идут хорошо. Количество алкилирующего реагента должно меняться в зависимости от того, какая степень алкилирования желательна. Обычно реакции ведут с молярными или меньшими количествами реагирующих веществ. [33]
Рассмотрим теперь мнения различных авторов о природе исследуемой полосы ацетона. Интенсивность и вид полосы кетонов в области 200 нм зависит от степени алкилирования [9, 10] и характера гибридизации [ II ] атома углерода карбонильной группы. Выводы работ [ 9, И ] сделаны в предположении, что исходной для данного электронного перехода является орбиталь п0 неподеленной пары атома кислорода, полностью локализованная на этом атоме. Однако в работе [12] при исследовании фотоэлектронных спектров ацетона и дейтероацетона замечено, что величина колебательного кванта вибронной структуры полос, отвечающих переходу электрона с орбитали п0 атома кислорода, испытывает изотопический эффект; это означает [ 131 что волновая функция исходной для рассматриваемого перехода орбитали имеет заметную плотность на метельных группах. Следовательно данная орбиталь не является чистой тг0 - орбиталью неподеленной пары атома кислорода, а содержит примесь орбиталвй ме-тильной группы. [34]
Получают их полимеризацией мономеров в органических растворителях или в блок с последующим подкислением или алкилированием. Регулируя процессы полимеризации и алкилирования, получают полимеры с различной молекулярной массой и степенью алкилирования. Растворяются в воде, метиловом и этиловом спиртах. [35]
 |
Зависимость средней величины алкиль-ного обрамления порфин-ного цикла в основных рядах от средней хроматографической подвижности концентрата нефтяных ванадилпорфиринов. [36] |
Сопоставляя масс-спектры концентратов с их распределением при ТСХ, можно отметить, что для нефтей с высоким набором молекулярных масс ванадилпорфиринов наблюдается также и наибольшая длина распределения их на хроматограмме, а с узким - наименьшая. Кроме того, прослеживается соответствие средней хроматографической подвижности концентрата ( полученной из величины Rf и относительного содержания фракций) со средней молекулярной массой и степенью алкилирования пор-фиринов. [37]
Однако указанная последовательность превращения первичной аминогруппы при действии алкилирующего средства вначале во вторичную, затем в третичную аминогруппу и, наконец, в четвертичное соединение совершенно необязательна. При действии на первичный амин алкилирующего средства, взятого даже без избытка против расчета на введение одного лишь алкила, возможно образование солеобразных продуктов всех степеней алкилирования, включая и четвертичное соединение при одновременном наличии и незатронутого исходного амина. [38]
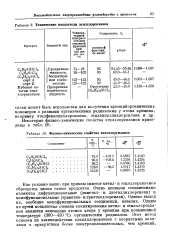 |
Технические показатели этвлхлорсилавов.| Физико-химические свойства этилхлорсиланов. [39] |
Как указано выше, при прямом синтезе метил - и этилхлорсиланов образуется целая гамма продуктов. Однако выход их, особенно монофункциональных соединений, невелик. Одним из путей повышения степени алкилирования метил - и этилхлорсиланов является замещение атомов хлора у кремния при повышенной температуре ( 300 - 450 С) органическим радикалом. [40]
Выходы при термических процессах очень ничтожные, и получаемые продукты в основном представляют собой полимеры. Выходы алкилата в каталитических процессах увеличиваются с повышением давления. Сравнение этих данных с данными, приведенными в табл. 4, показывает, что в одних и тех же условиях степень алкилирования пропиленом значительно ниже, чем степень алкилирования этиленом, что согласуется с приведенными выше термодинамическими расчетами. [41]
Выходы при термических процессах очень ничтожные, и получаемые продукты в основном представляют собой полимеры. Выходы алкилата в каталитических процессах увеличиваются с повышением давления. Сравнение этих данных с данными, приведенными в табл. 4, показывает, что в одних и тех же условиях степень алкилирования пропиленом значительно ниже, чем степень алкилирования этиленом, что согласуется с приведенными выше термодинамическими расчетами. [42]
В тех случаях, когда алкилирующий агент относительно летуч, для того чтобы реакция дошла до конца следует применять избыток реагента. Другой возможный вариант заключается в применении диметилсульфата, диэтилсульфата или подходящего алкилсульфоната. Иногда можно считать, что реакция закончена, если предоставить ей продолжаться до тех пор, пока реакционная смесь не станет нейтральной, однако во многих реакциях полной нейтральности достигнуть не удается, В таких случаях для определения степени алкилирования рекомендуется периодически отбирать аликвотные пробы реакционной смеси и титровать их стандартной кислотой. Чтобы упростить последующий процесс экстрагирования, большую часть спирта следует отгонять из реакционной смеси прежде. [43]
В тех случаях, когда алкилирующий агент относительно летуч, для того чтобы реакция дошла до конца следует применять избыток реагента. Другой возможный вариант заключается в применении диметилсульфата, диэтилсульфата или подходящего алкилсульфоната. Иногда можно считать, что реакция закончена, если предоставить ей продолжаться до тех пор, пока реакционная смесь не станет нейтральной, однако во многих реакциях полной нейтральности достигнуть не удается. В таких случаях для определения степени алкилирования рекомендуется периодически отбирать аликвотные пробы реакционной смеси и титровать их стандартной кислотой. Чтобы упростить последующий процесс экстрагирования, большую часть спирта следует отгонять из реакционной смеси прежде, чем вылизать ее в воду. [44]
При повышении температуры величина оптимального отношения Al / Ti увеличивается. Это подтвержается данными Ладлама и др. [279], которые показали, что для определенного соотношения Al / Ti при повышении температуры активность сначала возрастает, а затем при более высоких температурах резко падает. Оптимальная температура зависит от природы металлоорганических соединений и от молярного соотношения компонентов катализатора. Высказано предположение [279], что при повышении температуры возрастает степень алкилирования четырех-хлористого титана. При этом, по-видимому, происходит восстановление титана до валентностей более низких, чем в активном каталитическом комплексе. Согласно этой гипотезе, добавление при повышенных температурах в систему больших количеств алкила алюминия приводит к простому увеличению содержания этого вещества, причем алкилалюми-ний, вероятно, адсорбирован на поверхности соли титана. Если принять предположение Ладлама, Андерсона и Ашби [279], что активными центрами в реакции роста цепи являются атомы титана, то активность катализатора не должна зависеть от количеств алкила алюминия. [45]
Страницы: 1 2 3 4