Равновесная степень - конверсия
Cтраница 1
Равновесная степень конверсии зависит от температуры и состава газа. Равновесная степень превращения S02 в SO3 в газе, полученном от обжига пирита, показана на рис. III. В первом случае газ содержит 5; 7 и 9 % SO2 и во втором случае 7; 9 и 11 % SO2 и соответствующее количество кислорода в газе. [1]
Равновесная степень конверсии метана с ростом давления снижается, но путем повышения температуры и увеличения соотношения пар: газ можно уменьшить отрицательное влияние давления на конверсию углеводородов. [2]
Равновесная степень конверсии метана с возрастанием давления снижается, но путем повышения температуры и соотношения пар: газ можно уменьшить отрицательное влияние давления на реакции конверсии углеводородов. Однако возможность повышения температуры сверх 800 С в процессе конверсии под давлением ограничена механическими свойствами жаропрочных стальных труб, применяемых для изготовления трубчатых печей. Поэтому при паровой конверсии метана под давлением целесообразно более высокое соотношение пар: газ и допустимо большее остаточное содержание метана после первой ступени конверсии, чем на установках, работающих без давления. Во второй ступени, при конверсии метана воздухом, температура может быть повышена до 850 - 970 С, что позволяет увеличить степень конверсии до содержания не более 0 2 - 0 3 объемн. [3]
Другой метод повышения равновесной степени конверсии состоит в применении избытка водорода по сравнению со сте-хиометрическим, что широко используется для гидрирования в газовой фазе. [4]
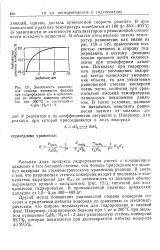 |
Зависимость равновесной степени конверсии бензола при гидрировании его в циклогек-сан от общего давления реагентов при 200 С и соотношении СеНй. Н2 1. 3. [5] |
Другой метод повышения равновесной степени конверсии состоит в применении избытка водорода по сравнению со стехиомет-рическим, что широко используется для гидрирования в газовой фазе. [6]
Эти методы повышения равновесной степени конверсии используют на практике тогда, когда термодинамические условия наименее выгодны для дегидрирования ( получение диенов и арилолефинов); в остальных процессах ( дегидрирование спиртов в карбонильные соединения, парафинов в моноолефины и др.) применяют атмосферное давление без разбавления реагентов. Процессы гидрирования из термодинамических соображений следует проводить при возможно более низкой температуре, позволяющей, однако, достичь приемлемой скорости реакции. В области относительно низких температур равновесие, как видно из рис. 114 и 115, практически полностью смещено в сторону гидрирования, и поэтому реакцию можно провести почти нацело при атмосферном давлении. По - скольку при гидрировании ( ввиду поглощения водорода) всегда происходит уменьшение объема, то для увеличения равновесной степени конверсии очень часто, особенно при сравнительно высоких температурах, используют повышенное давление. [7]
Другой корень дает равновесную степень конверсии ХА. [8]
Реакция обратима, причем равновесная степень конверсии составляет всего 12 % при 15 - 20 С и 16 % при 0 С. Такие невыгодные условия равновесия обусловлены тем, что в отличие от альдольных конденсаций альдегидов здесь не образуется ацеталей, способствующих сдвигу равновесия вправо. Конденсацию проводят при 0 - 20 С в присутствии едкого натра или нерастворимых гидроксидов кальция или бария, которые иногда рекомендуется применять на носителях. Реакционную массу нейтрализуют и перегоняют; при этом непревращенный ацетон регенерируется и возвращается на конденсацию. [9]
Реакция обратима, причем равновесная степень конверсии составляет всего 12 % при 15 - 20 С и 16 % при 0 С. Такие невыгодные условия равновесия обусловлены тем, что в отличие от реакций альдольной конденсации альдегидов здесь не образуется ацеталей, способствующих сдвигу равновесия вправо. Конденсацию проводят при 0 - 20 С в присутствии гидроксида натрия или нерастворимых гидроксидов кальция или бария, которые иногда рекомендуется применять на носителях. Реакционную массу нейтрализуют и перегоняют; при этом непревращенный ацетон регенерируется и возвращается на конденсацию. [10]
Реакция обратима, причем равновесная степень конверсии составляет всего 12 % при 15 - 20 С и 16 % при О С. Такие невыгодные условия равновесия обусловлены тем, что в отличие от альдольных конденсаций альдегидов здесь не образуется ацеталей, способствующих сдвигу равновесия вправо. Конденсацию проводят при 0 - 20 С в присутствии едкого натра или, лучше, нерастворимых гидроокисей кальция или бария, которые иногда рекомендуется применять на носителях. [11]
Реакция обратима, причем равновесная степень конверсии составляет всего 12 % при 15 - 20 С и 16 % при 0 С. Такие невыгодные условия равновесия обусловлены тем, что в отличие от альдольных конденсаций альдегидов здесь не образуется ацеталей, способствующих сдвигу равновесия вправо. Конденсацию проводят при 0 - 20 С в присутствии едкого натра или, лучше, нерастворимых гидроокисей кальция или бария, которые иногда рекомендуется применять на носителях. Реакционную массу нейтрализуют и перегоняют; при этом непревращенный ацетон регенерируется и возвращается на конденсацию. [12]
Разбавление паром, увеличивая равновесную степень конверсии, способствует росту селективности. Влияние температуры является двояким: с одной стороны, при ее повышении тоже растет равновесная степень конверсии, но, с другой, становятся более существенны некоторые побочные реакции, в том числе закоксовывание катализатора, снижающее его активность. [13]
Разбавление паром, увеличивая равновесную степень конверсии, способствует росту селективности, но влияние температуры является двояким. С одной стороны, при ее повышении тоже растет равновесная степень конверсии, но, с другой, становятся более существенны некоторые побочные реакции, в том числе закоксовывание катализатора, снижающее его активность. В результате имеется некоторый оптимум температуры дегидрирования: для этилбензола 580 - 600 С, для более реакцион-носпособного изопропилбензола 530 - 550 С. Кроме того, при каждых степени разбавления водяным паром и температуре имеется оптимум фактической степени конверсии, определяемый экономическими соображениями. [14]
Понижение температуры приводит к увеличению равновесной степени конверсии, но сильно замедляет скорость реакции даже на катализаторе. С увеличением отношения пар j газ степень превращения СО повышается. [15]
Страницы: 1 2 3 4