Равновесная степень - конверсия
Cтраница 2
Понижение температуры приводит к увеличению равновесной степени конверсии, но сильно замедляет скорость реакции даже на катализаторе. G увеличением отношения пар / газ степень превращения СО повышается. [16]
Понижение температуры приводит к увеличению равновесной степени конверсии, но сильно замедляет скорость реакции даже на катализаторе. [17]
 |
Зависимость равновесной мя п более низкой температуре. [18] |
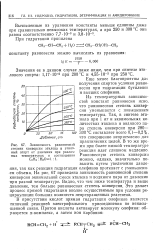
На рис. 67 приведена зависимость равновесной степени конверсии эквимольной смеси этилена и водяного пара от давления при разной температуре. Видно, что чем ниже температура и выше давление, тем больше равновесная степень конверсии. Это делает процесс прямой гидратации вполне осуществимым при условии рециркуляции больших количеств непревращенных реагентов. [19]
Для сравнения на рис. I представлена равновесная степень конверсии метана г р при температуре в реакторе. По мере продвижения смеси действительная степень конверсии приближается к павновесной, но не достигает ее. [20]
Следовательно разбавление паром, которое увеличивает равновесную степень конверсии, способствует росту селективности. Повышение температуры увеличивает как равновесную конверсию, так и выход побочных продуктов, в том числе кокса, за счет активизации побочных реакций. Оптимальными, таким образом, оказываются температурные условия 580 - 600 С, при которых одновременно обеспечиваются удовлетворительная конверсия и селективность. Следовательно, можно выбрать необходимые условия, позволяющие достигать экономически целесообразную степень конверсии. [21]
В последнее время разработан метод убыстренного расчета равновесных степеней конверсии для некоторых реакций в паровой и жидкой фазах, применяемых в нефтехимической технологии. [22]
Из температурных зависимостей констант равновесия ясно, что равновесная степень конверсии уменьшается с повышением температуры. Так, в синтезе этанола при 1 ат и эквимольных количествах этилена и водяного па - ра степень конверсии при 280 - Too 300 С составляет всего 0 1 - 0 2 %, что совершенно неприемлемо для практических целей. [23]
Такой же расчет для любой температуры показывает, что равновесная степень конверсии спирта в эфир очень мала, что как будто свидетельствует о невозможности получения эфира с хорошим выходом в системе таких параллельных реакций. В действительности это не так, и даже при одном и том же катализаторе удается направить процесс в ту или иную сторону, что зависит уже от кинетических факторов. Следовательно, для параллельных реакций термодинамика не может предсказать преобладающего направления превращений. [24]
Это предопределяет выбор общего давления 7 - 8 МПа, когда равновесная степень конверсии этилена равна 8 - 10 % Однако фактическую степень конверсии поддерживают на уровне 4 %, что позволяет работать при достаточно высоких объемной скорости ( 2000 ч -) и удельной производительности катализатора по спирту [ 180 - 220 кг / ( м3 - ч) ], получая после конденсации 15 % - й этанол. [25]
Из рассмотренного примера видно, что для газофазных реакций, не сопровождающихся изменением объема, равновесная степень конверсии не зависит от РА о. На нее влияет лишь избыток второго реагента Y, с увеличением которого растет и ХА. Это широко используют в технологии, когда применяют избыток более дешевого реагента для смещения равновесия. [26]
Принимаем, что степень конверсии хс в слое, примыкающем к поверхности трубы, равна равновесной степени конверсии при температуре стенки Тс. Степень конверсии в ядре потока хп определяется по анализу состава пирогаза в реакционной зоне. [27]
При получении а-метилсти-рола из изопропилбензола термодинамические отношения более благоприятны для дегидрирования: 50 % - ная равновесная степень конверсии при 1 кгс / см2 ( 0 1 МПа) достигается уже при 500 С, но и побочные реакции протекают в этом случае более интенсивно. [28]
В - отношение водород: углерод в сырье; А - количество инертных газов; Хр - равновесная степень конверсии СО. [29]
При получении а-метил стирол а из изопропилбензола термодинамические отношения более благоприятны для дегидрирования ( 50 % - ная равновесная степень конверсии при 1 ат достигается уже при 500 С), но и побочные реакции протекают в этом случае более интенсивно. [30]
Страницы: 1 2 3 4