Равновесная степень - конверсия
Cтраница 3
Из решения этого примера вытекает, что для реакций, не сопровождающихся изменением общего числа молей веществ, равновесная степень конверсии зависит не от давлений ( концентраций), а только от мольного соотношения реагентов: с его увеличением равновесная степень конверсии ключевого реагента повышается. Это влияние избытка одного из реагентов ( обычно более дешевого) широко применяется в промышленности и является общим для всех реакций между двумя или более реагентами, в том числе и для таких, где общее число молей изменяется. [31]
Обозначим: п - число грамм-молекул водяного пара, прибавляемого к 1 г-мол исходного сухого газа, Р - общее давление газа, пр - равновесная степень конверсии СО. [32]
Обозначим: п - число грамм-молекул водяного г / ара, прибавляемого к 1 г-мол исходного сухого газа, Р - общее давление газа, ар - равновесная степень конверсии СО. [33]
Вместо применения вакуума иногда удобно разбавлять реакционную массу газом или паром, инертным в условиях реакции, что также ведет к снижению парциальных давлений реагентов и росту равновесной степени конверсии. [34]
 |
Зависимость логарифма константы равновесия от обратной температуры. [35] |
Незначительное изменение KN при изменении исходного мольного соотношения реагентов более чем в три раза позволяет принять ее постоянной и использовать среднее значение KN 5 84 для расчета равновесных степеней конверсии. [36]
При этом, в отличие от олефинов, необходимо повышенное давление ( 1 - 5 МПа) - не только для ускорения реакции, но и для увеличения равновесной степени конверсии, так как термодинамические отношения в этом случае менее благоприятны для гидрирования. Ароматические углеводороды нужно предварительно очищать от соединений серы, являющихся контактными ядами. [37]
Незначительное изменение / Gv при изменении исходного мольного соотношения реагентов более чем в три раза позволяет принять ее постоянной и использовать среднее значение / Gv 5 84 для расчета равновесных степеней конверсии. [38]
Вместо того чтобы применять вакуум, иногда удобно разбавлять реакционную массу газом или паром, инертным в условиях реакции, что также ведет к снижению парциальных давлений реагентов и росту равновесной степени конверсии. Так как водород смещает равновесие в сторону гидрирования, а другие газы затрудняют выделение целевых продуктов, то на практике часто применяют перегретый водяной пар, сохраняя общее давление 0 1 МПа. [40]
 |
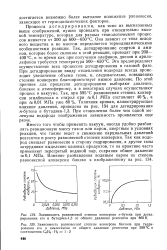
Зависимость равновесной степени конверсии бензола при гидрировании го в цнклогексан от общего давления реагентов при 200 С и соотношении С6Н6. Н21. 3. [41] |
Вместо того чтобы применять вакуум, иногда удобно разбавлять реакционную массу газом или паром, инертным в условиях ргакции, что также ведет к снижению парциальных давлений реагентов и росту равновесной степени конверсии. Так как водород смещает равновесие в сторону гидрирования, а другие газы затрудняют выделение целевых продуктов, то на практике часто применяют перегретый водяной пар, сохраняя общее давление ж 0 1 МПа. [42]
Наконец, при р 10 и общем давлении 1ОМПа ( 10 кгс / см2) находим ХА 0 999, что вытекает из общего принципа Ле-Шателье - Брауна о росте равновесной степени конверсии при повышенном давлении для реакций, идущих с уменьшением общего числа молей веществ. [43]
 |
Зависимость логарифма константы равновесия от обратной температуры. [44] |
Дальнейшая задача при расчете равновесий состоит в нахождении по найденным или вычисленным константам равновесия и заданным начальным условиям ( Рг -, о, С, 0) состава равновесных смесей и равновесных степеней конверсии. Рассмотрим вначале случай простых реакций. [45]
Страницы: 1 2 3 4