Стереоизомерия
Cтраница 4
Влияние стереоизомерии на органолептические свойства отчасти аналогично ее влиянию на химические свойства соединений. [46]
Понятие стереоизомерии, характерной для соединений с одинаковой системой связей, но различным расположением атомов в пространстве, вводится в связи с цис-транс-изомерией. [47]
Влияние стереоизомерии [111, 112] на распределение интен-сивностей в масс-спектрах обнаружено при исследовании изомеров диметилциклогексана. Так, например, вероятность отрыва метильной группы от 1 2-диметилциклогексана была на 35 % больше для грямс-изомеров; от 1 3-диметилциклогексана - на 20 % больше для ас-изомера; от 1 4-диметилциклогексана - на 7 % больше для транс-изомера. [48]
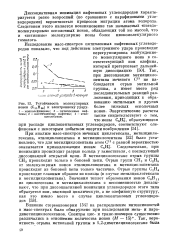 |
Устойчивость молекулярных ионов ( С1гН к электронному удару. [49] |
Влияние стереоизомерии [54] на распределение интенсивностей в масс-спектрах было обнаружено при исследовании мета - и пара-диметилциклогексанов. [50]
Открытие стереоизомерии показало, что в определенных случаях и структурная формула не полностью характеризует органическое вещество: чтобы охарактеризовать стереоизо-меры, необходимо знать их пространственную конфигурацию. При этом исторически сложилось так, что слово конфигурация вошло в органическую химию как довольно узко ограниченное понятие. Говоря о конфигурации, имеют ь виду пространственное расположение заместителей вокруг центра, обусловливающего возможность существования зеркальных форм, либо пространственное расположение заместителей относительно л-связи или относительно цикла. Таким образом, знание конфигурации совсем не равноценно раскрытию точной пространственной структуры всей молекулы в целом: оно относится только к упомянутым выше особым точкам в молекуле. [51]
Открытие стереоизомерии показало, что в определенных случаях и структурная формула не полностью характеризует органическое вещество; чтобы охарактеризовать стереоизомеры, необходимо знать их пространственную конфигурацию. При этом исторически сложилось так, что слово конфигурация вошло в органическую химию как довольно узко ограниченное понятие. Говоря о конфигурации, имеют в виду пространственную группировку вокруг центра, обуславливающего возможность существования зеркальных форм или quc - грамс-изомеров. [52]
Существование стереоизомерии у С5 было установлено Виндаусом [89] ( 1916 г.), а стереохимия ядер стероидов была впервые рассмотрена Ружичкой [90] ( 1933 г.), причем связь 6 асимметрических атомов ядра С5, С10, С8, С8, С14 и С13 была определена как транс-антпи-транс-анти - транс - в холестане и цис-анти-транс-апти - транс - в копростане. Результаты большой серии рентгенокристаллографических определений, проведенных Берналом [91] ( 1940 г.), дали общее подтверждение вышесказанному, но попытка Жакомелло [92] ( 1939 г.) вывести из данных рефракции рентгеновских лучей индивидуальные конфигурации у С12 и С17 в дезоксихолевой кислоте ( III; R Н) потерпела неудачу и привела к весьма запутанному положению, явившемуся следствием первоначальной интерпретации Рейхштейна [93] ( 1944 г.); это положение продолжалось до тех пор, пока Рейхштейн [94] ( 1946 г.), Галлагер [95] ( 1946 г.) и Кендалл [87] ( 1946 г.) независимо один от другого при помощи совершенно разных доказательств не внесли исправление. Существование естественной ( З - ориентации боковой цепи стероидов было доказано Карлилем и Кроуфутом [96] ( 1945 г.) полным рентгенокристаллографическим анализом йодистого холестерила. [53]
Страницы: 1 2 3 4