Стереоспецифичность
Cтраница 2
Стереоспецифичность определяется последующими реакциями находящихся на поверхности электрода карбанионов с растворителем или протоном. [16]
Стереоспецифичность многих метаболических реакций может объясняться причинами, имеющими отношение к формальным механизмам катализа. Например, одинаковая стереохимическая специфичность четырех кето-альдегид-изомераз привела Розе [13] к предположению об общем г с-эндиольном механизме для этих четырех ферментов и об одновременном разрыве связей в каждой из этих реакций. [17]
Стереоспецифичность этих реакций аналогична упомянутой выше. [18]
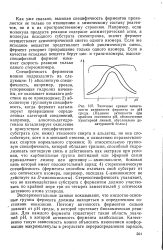 |
Типичные кривые зависимости активности фермента от рН среды. ( Падение активности при крайних значениях рН, обозначенное пунктирной линией, обусловлено денатурацией белка. [19] |
Стереоспецифичность указывает, что во взаимодействии субстрата с ферментом должно участвовать по крайней мере три из четырех заместителей у оптически активного атома углерода. [20]
Стереоспецифичность в таком случае можно рассматривать как результат структуры I, которая не допускает свободного вращения первого атома углерода в транс-положение относительно четвертого. Это ведет к тому, что с катализатора десорбируется и. Дис-изомер может затем адсорбироваться, присоединять протон, давая структуру II, которая уже легко может дать транс-изомер. [21]
Стереоспецифичность целиком зависит от асимметрии ядер дифеновой системы, а не от имеющегося в фенилдигид-ротебаине асимметрического атома, так как продукты превращения фенилдигидротебаина, не имеющие асимметрического атома, а обладающие лишь дифеновой асимметрией, также создают высокую Стереоспецифичность. [22]
Стереоспецифичность, наблюдаемая в этих реакциях объясняется существованием стабилизированного катионом мезомерного промежуточного карбаниона, подобного предложенному для изомеризации 1-бутена в ис-2 - бутен, но с участием кислородного атома. Независимо от механизма, очевидно, что эта реакция требует ifwc - конфигура-ции переходного состояния, поскольку там, где этого нельзя достигнуть, никакой изомеризации при тех же условиях не происходит. [23]
Стереоспецифичность можно исследовать только на тет-разамещенных олефинах ( кроме случаев, когда реагентом является D2), которые вступают в эту реакцию с наибольшим трудом. Однако полученные результаты показывают, что реакция на 80 - 100 % идет как сын-процесс, хотя обычно обнаруживается некоторое количество продуктов анты-присоединения, а в некоторых случаях эти продукты образуются преимущественно. Каталитическое гидрирование алкинов почти всегда идет стереоселективно, давая г ыс-олефин ( обычно не менее 80 %) даже в тех случаях, когда этот изомер термодинамически менее стабилен. [24]
Стереоспецифичность, обусловленную экранированием S jl - замещения, время от времени объясняют как замещение в ионных парах, включающих ион карбония. На самом деле она относится и ко многим другим случаям. [25]
Стереоспецифичность является еще более удивительной, если учесть то, что скорость обмена водорода у хирального бензильного атома углерода была гораздо больше, чем скорость изомеризации. [26]
Стереоспецифичность объясняется влиянием стерических факторов. [27]
Стереоспецифичность, несомненно, является одним из основных факторов в биологических реакциях - в ферментативных реакциях вообще и в специальном случае репликации ДНК путем спаривания дополнительных оснований из-за образования водородных связей. Но Стереоспецифичность сама по себе не объясняет, почему АТФ так часто принимает участие в реакциях, где не очевидно какое-либо специалъное участие самого аденина. Такой вид адсорбции сам по себе также не обязательно приводит к возникновению большой химической активности. Хорошо известна легкость, с которой реагирует хемосорбированный водород. Она обусловлена главным образом образованием атомов Н на поверхности. Но, по-видимому, нет очевидной причины, по которой дополнительные основания, удерживаемые на нуклеиновой кислоте водородными связями, должны особенно легко участвовать в реакциях поликонденсации. Однако если молекулы удерживаются в благоприятных положениях до тех пор, пока их соответствующие части не станут активными в результате перемещения свободных валентностей, которые, как мы видели, могли бы непрерывно распространяться по макромолекулярному остову клетки, то можно ожидать, что реакция и эффективная полимеризация будут происходить довольно легко. [28]
 |
Схема адсорбции субстра - - Адсорбционные. [29] |
Стереоспецифичность указывает, что во взаимодействии субстрата с ферментом должно участвовать по крайней мере три из четырех заместителей у оптически активного атома углерода. [30]
Страницы: 1 2 3 4