Стиси
Cтраница 1
Стиси и Элькин [423], сравнивая каталитическую активность поверхностей жидкого и твердого цинка, служащего катализатором при разложении метанола, указывают, что если указанная выше точка зрения верна, то плавление катализатора должно снижать его активность. [1]
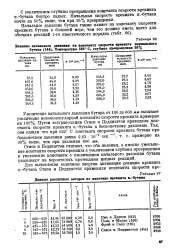 |
Данные различных авторов по кинетике крекинга н. - бутана. [2] |
Стиси и Педдингтон считают, что оба явления, а именно уменьшение константы скорости крекинга с увеличением глубины превращения и увеличение константы с увеличением начального давления бутана указывают на вероятность протекания цепных реакций. [3]
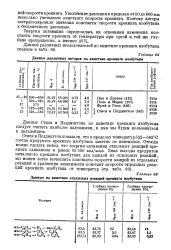 |
Данные различных авторов по кинетике крекинга изобутана.| Данные по кинетике отдельных реакций крекинга изобутана. [4] |
Стиси и Педдингтон показали, что в пределах температур 522 - 582 С состав продуктов крекинга изобутана заметно не изменялся. Отсюда можно сделать вывод, что энергии активации отдельных реакций крекинга одинаковы и равны 63 500 кал / моль. [5]
Стиси и Педдинг-тоном, примерно на 15 % выше константы, найденной Фрей и Гепп. [6]
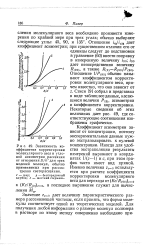 |
Зависимость коэффициента корректировки молекулярного веса и угловой асимметрии рассеяния от отношения D / X для трех моделей молекул, обычно применяемых при рассмотрении светорассеяния. [7] |
Стиси [9] собрал и представил в виде таблиц все данные, касающиеся величин Р ( в), асимметрии и коэффициента корректировки. Некоторые сведения об этих величинах дает рис. 49, где соответствующие соотношения изображены графически. [8]
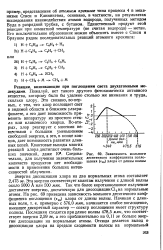 |
Зависимость мольного десятичного коэффициента поглощения ( EIO хлора от длины волны. [9] |
Стиси и Каннингема, основано, в частности, на результатах исследования взаимодействия атомов водорода, полученных методом Вуда в разрядной трубке, с бутаном. Единственный продукт этой реакции при комнатной температуре ( не считая водорода) - метан. [10]
Стиси и соавтор ( 140) показали, что добавка окиси азота не уничтожает полностью реакционных цепей, но лишь резко уменьшает их длину. Поэтому вычисляемая по Стевли и Гиншельвуду средняя длина реакционной цепи имеет обычно пониженное значение. [11]
Стиси удается связать скорость образования этилена со скоростью элементарной стадии распада радикала. Ясно, что величина предэкспонента 108 является константой не скорости элементарного акта, но константой скорости сложного брутто-процесса. [12]
Стиси [16] для реакции ( IX) дает значение энергии активации, равное 46 ккал / молъ. Энергия активации ( VII), согласно Дурхаму, Мартину и Саттону [25], 19 ккал / молъ, а по Стиси [16] значительно больше - 26 4; 4 ккал / молъ. Семенов [20], критически рассмотрев литературные данные, пришел к выводу, что энергия активации должна быть еще больше, а именно не ниже 30 ккал / молъ. [13]
Стиси и Фокине нашли также, что замедляющее влияние окиси азота уменьшается по мере увеличения давления бутана. Эт о указывает на то, что обрыв цепи происходит путем рекомбинации радикалов в присутствии молекул бутана в качестве третьего тела. [14]
 |
Изобары адсорбции диметилового эфира на алюминии вблизи критической температуры. [15] |
Страницы: 1 2 3 4