Стиси
Cтраница 2
Тап, Стиси и Маас [67] нашли что при нагревании системы жидкость - пар нельзя получить однородную фазу немедленно после того, как температура станет выше критической и исчезнет мениск; вместо этого образуется одна фаза более плотная и другая - менее плотная. Майер [58] объясняет это явление, применяя свою статистическую теорию конденсированных систем. [16]
Калверт, Стиси и др. [1052, 1051, 1050] предложили механизм фотолиза формальдегида и считают, что этому механизму лучше соответствует значение D ( Н - СНО) 91 ккал / моль. Доводы в пользу меньшего значения D ( Н - СНО) представляются более убедительными. Так, Горин [1826] исследовал процесс фотодиссоциации формальдегида в присутствии паров йода и показал, что энергия диссоциации связи Н - СНО должна быть менее 78 ккал / моль. [17]
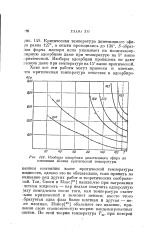 |
Изобары адсорбции диметилового эфира на алюминии вблизи критической температуры. [18] |
Тап, Стиси и Маас [67] нашли что при нагревании системы жидкость - пар нельзя получить однородную) азу немедленно после того, как температура станет: ыше критической и исчезнет мениск; вместо этого образуется одна фаза более плотная и другая - ме-юе плотная. Майер [58] объясняет это явление, применяя свою статистическую теорию конденсированных систем. [19]
Кальверт и Стиси [63] изучали фотохимическое разложение формальдегида в интервале 423 - 623 К. [20]
Форзит [50], а затем Дюрхем и Стиси [ 511 подробно исследовали ингибирующие свойства окиси азота методом Пакета с использованием теллурового зеркала. Во всех опытах скорость гибели свободных радикалов подчинялась закону первого порядка и была пропорциональна парциальному давлению окиси азота. Подсчитано, что из каждых 73 000 столкновений метильных радикалов с окисью азота эффективно одно. [21]
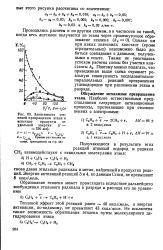 |
Зависимость степеней превращения этана в конечные продукты от удельной энергии ( / 350 ма. [22] |
Энергии активаций реакций 3 и 4, поданным Стиси, не превышают 8 ккал / моль. [23]
По данным Розенблюма [97], а также Джессера и Стиси [98], фотолиз смеси кетена с водородом при комнатной температуре или вовсе не приводит к получению метана, или же метан образуется в небольших количествах. [24]
Ошибка, вероятно, связана с тем, что Стиси измерял скорость указанной реакции распада радикала С3Н7 на СН3 и С2Н4 по выходу этилена. Между тем, фотосенсибилизирован-ные реакции крекинга представляют собой сложный процесс и лишь при определенных, видимо неверных, предположениях Стиси удается связать скорость образования этилена со скоростью элементарной стадии распада радикала. Ясно, что величина предэкспонента 108 является константой не скорости элементарного акта, но константой скорости сложного брутто-процесса. [25]
В отличие от результатов В. В. Воеводского и его сотрудников, Стиси и др. [133] нашли, что при генерировании радикалов СН3 и CgH путем фотолиза соответствующих кетонов, азо - и диалкилртутных соединений в присутствии молекулярного дейтерия получаются не глубоко обмененные продукты, а только монодейтерировапные вещества CH3D, G2H6D или продукты их последовательного замощения. [26]
Энергии активации реакций 3 и 4, по данным Стиси, не превышают 8 ккал / моль. [27]
Данные Фрей и Гепп, с одной стороны, и Стиси и Педдингтон, с другой, - показывают хорошую сходимость. [28]
Весьма подробную и тщательную работу по кинетике крекинга изобутана выполнили Стиси и Педдингтон ( 145) статическим методом ( описание метода см. выше, стр. [29]
Энергия активации реакции ( X), согласно Байуотеру и Стиси [23], равняется 39 5 ккал / молъ, а энергия активации реакции ( V), согласно Тротман-Диккенсону, Бирчарду и Стиси [24], - 8 0 ккал / молъ. [30]
Страницы: 1 2 3 4