Стиси
Cтраница 3
При исследовании полимеризации ацетилена под действием фотосенсибилизированных атомов ртути Ле-Рой и Стиси [2595] нашли для верхней границы D ( C2H - Н) значения 112 2 и 120 7 ккал / моль в зависимости от принимаемого механизма реакции. [31]
Изучая торможение окисью азота реакции крекинга бутана, сенсибилизированной распадающейся окисью этилена, Стиси и Фокине ( 139) пришли к выводу, - что окись азота не прекращает полностью цепных реакции, по только резко уменьшает их длину. Поэтому определяемая обычным методом средняя длина реакционной цепи имеет преуменьшенное значение. [32]
 |
Кинетика взаимодействия атомного водорода и дейтерия с молекулярным водородом и дейтерием. [33] |
Реакции с метаном, этаном, пропаном и нормальным изобутаном при комнатной температуре были изучены Стиси и Трестом. Они получили значения энергии активации 54 4 кДж - моль-1 для метана, около 37 7 кДж - моль 1 для этана и 41 8 кДж - моль 1 для пропана и обоих бутанов. Результаты более поздних работ не согласуются с этими цифрами. [34]
 |
Кинетика взаимодействия атомного водорода и дейтерия с молекулярным водородом и дейтерием. [35] |
Реакции с метаном, этаном, пропаном, нормальным и изобутаном при комнатной температуре были изучены Стиси и Трестом. Они получили значения энергии активации 54 4 кДж / моль для метана, около 37 7 кДж / моль для этана и 41 8 кДж / моль для пропана и обоих бутанов. Результаты более поздних работ не согласуются с этими цифрами. [36]
Таким образом можно объяснить, почему Бон и Хилл в этанокис-лоролных смесях наблюдали воспламенение при прибанлении % ацеталь-дегида, тогда как Стиси и Плгсис этого 44екта не обнаружили - первые авторы работали пги 31Ь С, последние - при 452 С. [37]
В ряде тщательных работ по крекингу пропана и обоих изомерных бутанов, выполненных статических методом с полным анализом продуктов крекинга, Стиси и соавторы ( 144, 145, 146) также обнаружили уменьшение константы скорости крекинга указанных углеводородов по мере увеличения глублны превращения и также объясняют это явление наличием цепных реакций. Таким образом для газообразных парафиновых углеводородов явление самоторможения реакции крекинга может считаться достаточно твердо установленным, по крайней мере для крекинга при нормальном или пониженном давлении. [38]
Энергия активации реакции ( X), согласно Байуотеру и Стиси [23], равняется 39 5 ккал / молъ, а энергия активации реакции ( V), согласно Тротман-Диккенсону, Бирчарду и Стиси [24], - 8 0 ккал / молъ. [39]
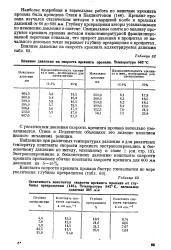 |
Влияние давления на скорость крекинга пропана. Температура 662 С. [40] |
С увеличением давления скорость крекинга пропана несколько увеличивается. Стиси и Педдингтон объясняют это явление наличием цепного механизма реакции. [41]
Между данными различных авторов наблюдаются значительные расхождения. Стиси и Педдингтон считают, что вычисление энергии активации на основании констант скорости крекинга бутана при атмосферном давлении ( а не экстраполированных к бесконечному давлению) приводит к ошибке на 1 7 Кал в сторону преувеличения. [42]
Энергия активации распада радикала СН3СО на СН3 и СО, согласно измерениям разных авторов, колеблется между 10 и 20 ккал. Стиси [10], анализируя экспериментальные данные, приходит к заключению, что наиболее вероятным является значение е 18 ккал. [43]
Дургамом, Мартином и Саттеном [125] энергия активации этого процесса ( 19 - 20 ккал) неверна. Стиси и Мандель-корн, изучая фотолиз ацетона в присутствии этилена, нашли сравнительно высокое ( 7 ккал) значение энергии активации, обратной распаду реакции присоединения радикала СН3 к этилену. Ранее, обычно, всеми авторами энергия активации этой реакции принималась равной 2 - 3 ккал. [44]
Хорошим критерием степени дробления молекулы при крекинге является число молекул, образующихся из одной молекулы исходного парафинового углеводорода. Стиси и соавторы ( 144, 146, 146) показали, что простейшие парафиновые углеводороды ( пропан, бутан, изобутан) при давлении 50 - 600 мм и температуре 500 - 600 С дают точно 2 молекулы на каждую распавшуюся молекулу исходного углеводорода. При увеличении молекулярного веса огромное влияние на степень распада парафиновых углеводородов начинает оказывать давление. [45]
Страницы: 1 2 3 4