Изменение - пересыщение
Cтраница 4
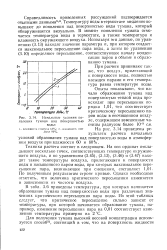
Изменение концентрации растЕора при движении через псевдоожи-женный слой подчиняется экспоненциальному закону ( рис. 22), причем величина пересыщения раствора после кристаллорастителя не превышает Ъ % предельного пересыщения данного раствора. Так как каждое вещество характеризуется величиной предельного пересыщения, то существует и предельная высота псевдоокнженного слоя, на которой изменение пересыщения составляет 95 предельного. [46]
 |
Начальные условия появления тумана над поверхностью. [47] |
В табл. 3.6 приведены температуры, при которых начинается образование тумана над поверхностью воды при различных значениях критического пересыщения пара воды. Из этой таблицы следует, что критическое пересыщение сильно зависит от температуры, при которой начинается образование тумана, например, изменение пересыщения пара на 0 01 соответствует изменению температуры примерно на 2 С. [48]
При производстве экстракционной фосфорной кислоты важной является скорость превращения одной модификации сульфата кальция в другую. Этот процесс в водных растворах связан с одновременным течением процессов растворения и кристаллизации, с влиянием твердых частиц на скорость зародышеобразова-ния и характер изменения пересыщения. [49]
В предыдущем сообщении [ J ] приводились соображения относительно характера изменения пересыщения раствора в процессе совместной кристаллизации азотнокислого калия и бихромата калия. На основании этих соображений объяснялось влияние бихромата калия на кристаллизацию KN03 - Для проверки сделанных нами ранее предположений были проведены дополнительные исследования, позволяющие установить ход изменения пересыщения раствора по отношению как к азотнокислому калию, так и к бихромату калия. Результаты этих исследований приводятся в данной работе. Кроме того, приводится вывод приближенного уравнения, связывающего степень захвата примесей с исходным составом раствора. Наличие такой связи было подтверждено экспериментально в ранее опубликованных работах I1 3 ], в которых было установлено, что коэффициент захвата примесей К остается почти постоянным. [50]
При небольших пересыщениях дает хорошие кристаллы. Чувствителен к изменению пересыщения, что выражается в захвате включений раствора. Удобен для изучения температурных аномалий скоростей поста. [51]
По мере хода химической реакции концентрация SO - медленно растет, пока произведение [ Ва2 ] [ SO - ] не достигнет критического значения, соответствующего образованию зародышей кристаллического сульфата бария, после чего раствор быстро мутнеет. В другом примере образующаяся в подкисленном растворе тиосульфата сера остается гомогенно-растворенной, пока не будет достигнуто критическое пересыщение. Для таких простых последовательных реакций ход изменения пересыщения, скорости образования зародышей и роста объема новой фазы представлен схематически на рис. 7, а, б, в. При построении графика 7, в сделано предположение, что размер частиц новой фазы линейно возрастает со временем. [52]
С точки зрения диффузионной теории трудно объяснить, почему шар, выточенный из кристалла и помещенный в пересыщенный раствор, растет в нем уже в виде многогранника [155, 156] с различной скоростью роста отдельных граней. Установлено также, что для одной и той же соли изменение пересыщения при различной температуре может по-разному влиять на скорость роста. [53]
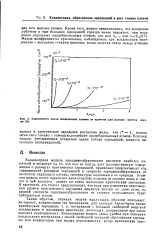 |
Зависимость числа осажденных атомов от времени для разных времен жизни. [54] |
Капиллярная модель зародышеобразования является наиболее понятной и несмотря на то, что она не всегда дает количественную информацию о размерах критических зародышей, правильно предсказывает ход зависимостей размеров зародышей и скорости зародышеобразования от величины падающего потока, температуры подложки и ее природы. Атомная модель почти идентична капиллярной; отличие ее состоит лишь в том, что в ней делается акцент на очень маленькие критические зародыши. В частности, эта теория предсказывает, что если при изменении пересыщения размер критического зародыша меняется только на один атом, на кривой скорости зародышеобразования от степени пересыщения будет наблюдаться излом. [55]
Кинетика образования осадка в принципе может быть описана любым из приведенных в главе V уравнений. При таком допущении уравнения могут быть использованы для описания кинетики кристаллизации в интервале изменения пересыщений, начало которого отвечает достижению максимальной скорости кристаллизации. [56]
Судя по данным таблицы, ширина метастабильной зоны сравнительно мало зависит от температуры. Зато величина tjnu и функция t - mu - - - f ( c0 / ceq) находятся с ней в прямой связи. Чем выше температура, тем в большей степени изменяется продолжительность индукционного периода с изменением пересыщения. Об этом свидетельствует рост кажущегося порядка процесса за-родышеобразования. [57]
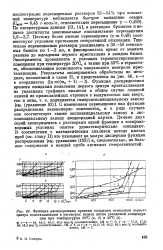 |
Функция распределения времени ожидания появления первого центра кристаллизации в растворах иодата лития различной концентрации при температурах 20 С ( а, б и 40 С ( в. [58] |
Поэтому более низкие пересыщения ( 7 J 0 49) соответствуют условиям протекания гетерогенной нуклеации. Тщательно перемешанные растворы разливались в 30 - 40 стеклянных бюксов по 1 - 2 мл; и фиксировалось время от момента разлива до выпадения первого кристаллика в каждом бюксе. Эксперименты проводились в условиях термостатированного помещения при температуре 20 G j а также при 40 G в термоста-тел обеспечивающем возможность визуального контроля кристаллизации. С изменением пересыщения вид функции распределения закономерно изменяется и в ряде случаев она соответствует также экспоненциальному закону и экспоненциальному закону неоднородной партии. Данные двух серий экспериментов с растворами одной фракции в воспроизводимых условиях опытов удовлетворительно совпадают. В соответствии с математическим анализом метода многих проб ( см. главу II) это указывает на малую дисперсию функции распределения [ см. уравнение ( 185) I иг следовательно, на большое содержание в каждой пробе активных гетерогенностей. [59]
Добавление в раствор кристаллов в большем количестве ( Р 5 %) приводит к тому, что средний размер частиц в продукте уже практически не зависит от темпов охлаждения раствора и оказывается больше его значения по сравнению с кристаллизацией без затравки. Причем средний размер получаемых кристаллов оказывается довольно близким к его значению для затравочных кристаллов. При увеличении интенсивности охлаждения, а следовательно, и пересыщения при кристаллизации, с одной стороны, возрастает скорость роста затравочных кристаллов, а с другой - еще в большей степени увеличивается скорость образования новых зародышей. Оба фактора, по-видимому, перекрывают друг друга в интервале испытанных значений 9, поэтому изменение скорости охлаждения и связанное с этим изменение пересыщения раствора не оказывает заметного влияния на величину dcv получаемых кристаллов. [60]
Страницы: 1 2 3 4 5