Стрептидин
Cтраница 3
Окончательным решением вопроса о строении и пространственной структуре стрептидина явился его синтез ( Вольфрам, 1948 - 1950), в ходе которого установлено, что последнему соответствует транс-конфигурация каждого заместителя. [31]
Последний под влиянием вновь образовавшейся кетогруппы отщепляет N-метилглюкозамин, а затем стрептидин, образуя мальтол. [32]
Остаток стрептобиозамнна присоединен через глюкозь-дный атом остатка стрептозы к четвертому атому стрептидина. [33]
Остаток стрептобиозамина присоединен через глкжозидный атом остатка стрептозы к четвертому атому стрептидина. [34]
Для того чтобы иметь возможность использовать эту реакцию для изучения строения стрептидина, было необходимо предварительно выяснить вопрос о расщепляемости йодной кислотой соединений, имеющих рядом с гидроксилом остаток гуаницина. [35]
Получен ряд солей стрептидина: хлоргидрат, сульфат, хлоро-платинат и др. Стрептидин не дает реакций на кетонную группу и первичную аминогруппу. [36]
При этом следует отметить, что факт присоединения маннозидострептобиозамина к С4 остатка стрептидина был доказан и химически476 - с этой целью из маннозидострептомицина было получено его тетрадекабензоильное производное, расщепленное затем НВг до гептабензоилстрептидина ( 58) ( см. схему 10), ранее уже полученного аналогичным путем из стрептидина ( ср. Следовательно, маннозидострептомицин отличается от стрептомицина лишь наличием остатка D-маннозы, присоединенного гликозидной связью к одному из углеродных атомов М - метил-1. [37]
Для окончательного выяснения строения стрептомицина необходимо было установить, к какому именно углеродному атому стрептидина присоединен стрептобиозамин. [38]
Как уже отмечалось выше, ряд данных определенно указывает, что связь между остатками стрептидина и стрептобиозамина осуществляется в стрептомицине за счет гликоэидного гидроксила стрептозной части молекулы. Из двух возможных формул - ( 56) и ( 57), удовлетворяющих этому условию, свойствам антибиотика отвечает только вторая формула ( 57), тогда как первая ( в которой отсутствует свободная альдегидная группа) не может объяснить легкой восстанавливаемости стрептомицина в дигидрострептомицин ( см. ниже) и его способности вступать во взаимодействие с реагентами на карбонильную группу. [39]
Вопрос о том, в какой последовательности соединены между собой в молекуле маннозидострептомицина остатки стрептидина, стрепто - биозамина и маннозы, был решен двумя различными приемами. [40]
Прежде всего следует остановиться на тех работах, которые касаются синтеза и установления пространственного строения стрептидина. [41]
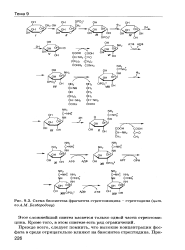 |
Схема биосинтеза фрагмента стрептомицина - стрептидина ( цит. по A.M. Безбородову. [42] |
Прежде всего, следует помнить, что высокие концентрации фосфата в среде отрицательно влияют на биосинтез стрептидина. [43]
Одновременно был изучен и ряд других превращений стрептомицина, что позволило выяснить, каким образом остатки стрептидина и стрептобиозамина соедииены между собой в молекуле антибиотика. Таким образом, стрептомицин представляет собой N-метил-а - - глю-козаминидо - р - - отрепто Зидо-стрептидин. [44]
При кипячении стрептидина в течение 1 часа с раствором гидрата окиси бария происходит отщепление 2 молей аммиака ( на 1 моль стрептидина) и образуется нейтральное кристаллическое вещество, представляющее собой производное мочевины; оно получило название стрептомочевины ( 216) ( см. схему 14, стр. [45]
Страницы: 1 2 3 4