Электронное строение
Cтраница 1
Электронное строение карбенов и их реакционная способность. [1]
Электронное строение лиганда опреде - Электронные ляет характер связи его с центральным пигандов атомом. [2]
Электронное строение ХеР2 и Kjp2 рассмотрено в начале этой главы. [3]
Электронное строение еще сложнее у антрацена и изомерного ему фе-нантрена. Рентгеноструктурный метод оказывается недостаточно чувствительным для характеристики электронного состояния связей С-С в конденсированных аренах. С-С - связи узловых атомов ( их четыре, а у нафталина - два) и Ci - C3, C6 - C7 имеют почти одинаковую длину, что не может быть объяснено анализом тс-электронного взаимодействия и для отдельной молекулы маловероятно. Очевидно следует учесть, что рент-геноструктурный анализ дает нам сведения не о независимой молекуле, а о молекуле в твердой фазе, в которой она искажается за счет довольно значительных сил межмолекулярного взаимодействия. [4]
Электронное строение характеризует распределение электронной плотности атомов в свободном и связанном состоянии. [5]
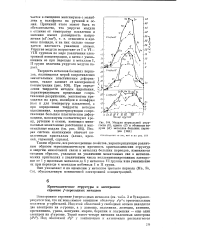 |
Модули нормальной упругости ( Е, сдвига ( G и объемные мо-дулп ( К металлов больших периодов. [6] |
Электронное строение / - переходных металлов ( см. табл. 3 и 9) характеризуется тем, что их ионы имеют внешнюю оболочку s2p6 с ортогональным секстетом р-орбиталей. Над этой оболочкой у свободных атомов находятся два электрона на s - уровне, а у лантана, гадолиния, лютеция, актиния, протактиния, урана, нептуния, кюрия, берклия и лоуренсия - еще один электрон на d - уровне. [7]
Электронное строение / - переходных металлов характеризуется тем, что они имеют два или три электрона на внешних d - и s - уровнях, под которыми располагается заполненная 2рв - оболочка иона. На более глубоких уровнях - 4 / и 5 / - размещается остальная часть электронов. [8]
Электронное строение всех этих комплексов имеет так много общих черт, что целесообразно на них и остановиться. [9]
Электронное строение диазометана описывается набором резонансных структур, две из которых приведены ниже ( подробнее о строении диазоал-канов см. в разд. [10]
Электронное строение и свойства молекулы ( или молекулярной системы) в любом из ее возможных стационарных состояний могут быть, в принципе, определены решением стационарного уравнения Шредингера. [11]
Электронное строение октаэдрическн координированного иона с конфигурацией d 2, типичным представителем которого является Vй1, уже обсуждалось в гл. [12]
Электронное строение Vй идентично электронному строению Сгш, поэтому они имеют аналогичные диаграммы энергетических уровней ( см. на стр. [13]
Электронное строение соединении марганца ( П) представляет большой интерес, поскольку на их примере можно довольно четко продемонстрировать некоторые важнейшие положения теории. [14]
Электронное строение ( или, иными словами, конфигурация ос новного состояния и соответствующие потенциалы ионизации молекул О2, N2 и СО хорошо изучено в более ранних работах [17] и эти вещества представляют интерес для исследования возможное тей метода фотоэлектронной спектроскопии. [15]
Страницы: 1 2 3 4