Влияние - алкильный заместитель
Cтраница 3
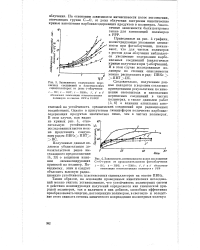 |
Зависимость содержания пере.| Зависимость интенсивности полос поглощения. [31] |
Следовательно, полученные данные находятся в хорошем согласии с приведенными результатами по изменению световыхода и накоплению перекисных соединений в чистых полимерах, а также данными работ [5, 6] о влиянии алкильных заместителей на устойчивость органических соединений при радиационных воздействиях. Однако в присутствии люминофоров количество карбонилсодержащих продуктов значительно ниже, чем в чистых полимерах. В этом случае, как видно из кривых рис. 4, отно - 60г сительную устойчивость исследованных систем можно представить следующим рядом: ПВКс ПВТ ПС. [32]
При изучении химии парофазной гидрогенизации на промышленных сульфидных катализаторах наибольший интерес представляет выяснение влияния заместителей на скорость и направление отдельных реакций процесса - реакций гидрирования, изомеризации и расщепления. Влияние алкильных заместителей на скорость гидрирования бензольного кольца рассмотрено выше ( см. гл. [33]
Влияние алкильных заместителей рассматривают как аддитивное. Суммирование проводят по всем атомам г, содержащим заместитель. [34]
Определено также влияние алкильных заместителей в пиридиновом кольце на глубину превращения в парафины. [35]
Этим обусловлен тот факт, что такие мономеры, как изобутилен, стирол, метилвиниловый эфир и изопрен, полимеризуются в присутствии катионных инициаторов. Значительно менее выражено влияние алкильных заместителей в катионной полимеризации, поэтому только 1 1-дизамещенные алкены полимеризуются по катионному механизму. [36]
Среди последних 4-метилзамещенные соединения обладают наибольшей ингибирующей способностью. Однако далеко не всегда сразу удается выявить влияние алкильных заместителей на эффективность фенолов. Ниже приведены результаты, полученные при старении полиэтилена высокого давления, стабилизированного добавкой 0 01 вес. [37]
При благоприятных геометрических условиях возможно перекрывание орбиталей я-электронов двойной связи с орбиталями а-электронов соседних групп - так называемое сверхсопряжение. Примером этого явления может служить повышение стабильности двойной связи под влиянием алкильных заместителей. [38]
Однако наиболее легко они протекают в случае 4-за-мещенных пространственно-затрудненных фенолов и являются характерной особенностью фенольных соединений данного типа. Превращение пространственно-затрудненных фенолов в различные циклогексадиеноны в значительной степени облегчено стериче-ским влиянием алкильных заместителей, которые, с одной стороны, способствуют отщеплению протона от гидроксильной группы, а с другой - увеличивают стабильность получающихся хинолидных соединений, пространственно экранируя карбонильную группу. Замещение атома водорода в мета-положении у 2 4 6-триалкилфенолов становится иногда возможным лишь при наличии в орто-положениях неразветвленных алкильных заместителей. [39]
Такое изменение положения длинноволновой полосы должно отражаться ЛКАО МО моделью катиона, что и наблюдается в действительности. Как будет видно далее, поведение длинноволновой полосы 351 M [ i катиона азуления под влиянием алкильных заместителей настолько хорошо согласуется с предсказаниями ЛКАО МО расчета для катиона XLIX, что эта структура и должна быть приписана катиону азуления. [40]
Понятие индуктивный эффект достаточно хорошо обосновано экспериментально и является очень полезным для химиков-органиков, однако стало очевидным, что алкильные группы способны стабилизовать не только положительные, но и отрицательные ионы. Это следует из характера кислотности спиртов в газовой фазе [139, 140] ( ВиОН ЕЮН МеОН Н20) и влияния алкильных заместителей на увеличение силы кислоты в растворе. [41]
Нетрудно видеть, что процесс образования переходного комплекса из-за большого объема катализатора будет чрезвычайно чувствителен к стерическим факторам. Экранирование двойной связи приводит к тому, что эпоксидирование протекает преимущественно или исключительно со стороны, свободной от влияния алкильных заместителей. [42]
Ими изучены также низкомолекулярные структурные аналоги указанных полимеров ( Г - изопропил - валеролактам, бутиролак-там, пирролидон - К-уксусная кислота) и сополимер винилпирро-лидона с малеиновым ангидридом. Было показано, что при гидролизе полимерных лактамов, так же как и их низкомолекулярных аналогов, большое значение имеет влияние алкильного заместителя у азота лактамного кольца. Поведение поливинилпирролидона в условиях щелочного гидролиза близко к поведению N-изопропил - 7-валеролактама. Карбоксильная группа, стоящая рядом с лак-тамным кольцом ( в пирролидон - К-уксусной кислоте), повышает склонность лактамного цикла к гидролизу, а наличие алкильной группы понижает ее. Этим объясняется, например, высокое значение энергии активации гидролиза поливинилпирролидона. Так, константа скорости гидролиза при 100 С в 1 N NaOH равна 4 5 10 - - лшн 1, а энергия активации 25 1 ккал / молъ. [43]
ЛКАО МО моделью катиона, что и наблюдается в действительности. I 145j3 по сравнению с 0 877 5 для азуленя ( см, табл. 2), Как будет видно далее, поведение длинноволновой полосы 351 MI катиона азуления под влиянием алкильных заместителей настолько хорошо согласуется с предсказаниями ЛКАО МО расчета для катиона XLIX, что эта структура и должна быть приписана катиону азуления. [44]
Способность ацилмалонового эфира енолизоваться определяется большой подвижностью водорода в остатке малонового эфира из-за присутствия трех сильных электроотрицательных групп. Замена метильной группы на какую-либо алкильную группу мало сказывается на протонизации водорода в метиновой группировке. Влияние алкильных заместителей определяется в основном их сте-рическими эффектами. Пространственное взаимодействие R с большой сложноэфирной группой должно дестабилизировать енол. [45]
Страницы: 1 2 3 4