Влияние - электронный фактор
Cтраница 1
Влияние электронных факторов на скорость реакции хорошо видно на примере гидролиза гликозидов аминосахаров и 2-дезоксиальдоз. Так, высокая устойчивость к гидролизу гликозидов аминосахаров связана с тем, что на аминогруппе в кислой среде возникает положительный заряд, затрудняющий протонирование атома кислорода и дестабилизующии гликозил-катион X. В 2-дезоксиальдоз ах, напротив, отсутствует индукционный эффект гидроксильной группы при С2, который снижает электронную плотность при гликозидном центре, затрудняет образование оксониевого иона и дестабилизует гликозил-катион. [1]
Влияние электронного фактора в гетерогенном катализе очень часто не проявляется вследствие того, что процесс промотирования, который определяет концентрацию электронов или дырок в катализаторах, может изменить и другие параметры кристалла, влияющие на каталитическую активность. Таким образом, для выяснения влияния электронного фактора необходимо выбирать только такие катализаторы, которые получены одним и тем же способом. [2]
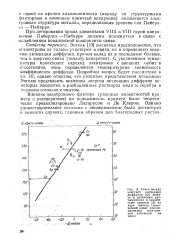 |
Связь между энергией активации диффузии ( Q железа в различных растворителях и химическим сдвигом ( б на ядре железа ( химический сдвиг пропорционален электронной плотности на ядре. [3] |
Влияние электронного фактора ( разницы валентностей примеси и растворителя) на подвижность примеси было теоретически проанализировано Лазарусом и Ле Клером. [4]
Влияние электронного фактора в гетерогенном катализе очень часто не проявляется вследствие того, что процесс промотирования, который определяет концентрацию электронов или дырок в катализаторах, может изменить и другие параметры кристалла, влияющие на каталитическую активность. Таким образом, для выяснения влияния электронного фактора необходимо выбирать только такие катализаторы, которые получены одним и тем же способом. [5]
Влияние электронных факторов на закономерности адсорбции может проявляться, в частности, в специфическом эффекте взаимного влияния адсорбированных частиц, связанных с твердым телом. Природа такого влияния кратко обсуждалась выше. [6]
Однако влияние электронных факторов на реакционную способность карбонила в большинстве случаев менее значительно, чем влияние пространственных факторов, потому что реакции присоединения к карбонилу очень чувствительны к пространственным помехам. [7]
Рассматривается влияние электронного фактора в реакциях высокотемпературного окисления СО и Н2 на катализаторах из закиси никеля, непромотированной и промотированной окисью лития или окисью галлия. Обсуждение результатов проведено на основании улучшенной теории, базирующейся на новы. [8]
Рассматривается влияние электронных факторов в процессе адсорбции и при катализе на металлах и полупроводниках. Сопоставлена роль коллективных и локальных взаимодействий в катализе. На основе координационных представлений освещены общие закономерности гетерогенного, гомогенного и ферментативного катализов. [9]
Разумеется, влияние электронных факторов на скорость процесса было бы недостаточно сводить лишь к влиянию изменений работы выхода электрона. Особенно следует иметь в виду также, что всякие изменения величин теплот адсорбции за счет - электронных факторов вне оптимального интервала этих величин могут снижать скорость реакции. [10]
Очевидно, влияние электронных факторов на скорость реакции должно существенно зависеть от характера лимитирующей стадии процесса. С другой стороны, изменение Ф, влияя на прочность адсорбционной связи, может приводить и к снижению скоростей других быстрых стадий. Следовательно, если быстрой стадией является взаимодействие адсорбированного вещества с другим компонентом из газовой фазы, то эта быстрая стадия из-за изменения Ф может стать медленной. Фактором, регулирующим такие изменения, может быть введение в катализатор определенных добавок, влияющих на его электронную структуру. [11]
Ярким примером влияния электронного фактора на основность и нуклеофильность аминогруппы является практически полное отсутствие указанных свойств в амидах карбоновых кислот, в молекулах которых аминогруппа непосредственно связана с электроноакцепторной ацильной группой. [12]
Количественная трактовка влияния электронных факторов на кинетику реакций в присутствии полупроводниковых катализаторов дана С. При более точном рассмотрении необходимо также учитывать взаимное наложение и влияние обоих факторов. Аналогичным образом обстоит дело и в случае взаимодействия адсорбированных частиц. [13]
Наряду с влиянием электронных факторов для хода реакции существенное значение имеет пространственное строение алкиль-ного остатка субстрата. Для образования переходного состояния в реакции типа SN2 нуклеофильный реагент должен уже известным способом ( разд. Этот процесс, однако, затрудняется, по мере того как объемистые заместители; заслоняют углеродный атом. [14]
Таким образом, влияние электронного фактора на градиент электрического поля и, соответственно, на направление сдвига частоты может быть неодинаковым в разных типах комплексов. Количественная мера этого влияния определяется преимущественно степенью переноса заряда. [15]
Страницы: 1 2 3 4