Влияние - карбоксильная группа
Cтраница 3
Иногда производные хроматографируют, чтобы добиться падежной идентификации; например, у стероидных спиртов значения Hf должны совпадать с значениями Rf их ацетатов. После устранения влияния карбоксильных групп в порфпринах ( этерификацией) па процесс хроматографии начинают оказывать влияние другие структурные особенности молекулы. К наибольшим успехам к области химии белков принадлежит разработка метода структурного анализа, в котором концевые аминокислоты превращаются в характерные производные, которые и подвергают хрома-тографированию ( см. стр. [31]
Влияние гидроксильных групп сильно снижается при образовании простых и сложных эфиров. Этерификация снижает также влияние карбоксильной группы. Гидроксильная и карбоксильная группы действуют на адсорбируемость сильнее карбонильной, карбонильная-сильнее ацетильной, ацетильная-сильнее нитро-группы. Тиокарбонильная группа уступает карбонильной, родано-группа действует слабее нитрильной. [32]
Если при охлаждении льдом в течение 20 мин s раствор р-бензоплакрилово. В этом случае ( i-ориептирующее влияние кетогруппы преобладает - над влияние карбоксильной группы. [33]
По отношению к родану это влияние особенно значительно. Если влияние карбиполыюй группы исчезает при перемещении двойной связи в р, у-положение, то влияние карбоксильной группы ( см. табл. 4) распространяется и на более удаленные двойные связи. [34]
Из оксикислот путем отнятия воды могут получаться непредельные кислоты. Особенно легко дегидратации подвергаются 8-оксикислоты так как в этих соединениях атом водорода в а-положении под влиянием карбоксильной группы обладает повышенной подвижностью, что и облегчает выделение воды. Поэтому 5-оксикислоты уже при нагревании даже в отсутствии водоотнимающих средств превращаются в непредельные кислоты. [35]
Из оксикислот путем отнятия воды могут получаться непредельные кислоты. Особенно легко дегидратации подвергаются - Оксикислоты, так как в этих соединениях атом водорода в а-положении под влиянием карбоксильной группы обладает повышенной подвижностью, что и облегчает выделение воды. [36]
Кривая титрования смеси НС1 и аминоуксусной кислоты ( см. рис. 31, кривая 6) имеет другой характер. Хотя электропроводность раствора до первой точки эквивалентности также понижается, кривая титрования на этом участке изогнута, что соответствует влиянию карбоксильных групп катионов амфолита. На втором участке кондукто-метрической кривой, соответствующем взаимодействию цвиттер-ионов, происходит линейное повышение проводимости. Участок кривой до первого излома дает возможность рассчитать содержание в смеси НС1, а между первым и вторым изломами - содержание аминоуксусной кислоты. Избыток основания при титровании всех перечисленных смесей вызывает резкое повышение электропроводности раствора. [37]
Однако и в этом случае получен только ад-дукт ( LXXI) с карбоксильной группой в орто-положении 201; таким образом, влияние карбоксильной группы на структуро-образование намного превосходило влияние метильного радикала. [38]
Нирочом, соответствующие, опыгы проведены с веществами, имеющими относительно короткую пень атомов углерода, а именно; пентеновыми кислотами. COOH обусловливается ие обращением влияния карбоксильной группы, а тем, что в конечной пи пильной группе в соответствий с приведенным выше правилом галоген присоединяется к атому углерода, более бедному водородом. [39]
В процессе обсуждения удобно опираться на частный пример. Так как читателю ближе знакома химия, рассмотрим сложный эфир в качестве субстрата и карбоксильную группу в качестве катализатора. Экспериментальный подход весьма прост - необходимо наблюдать влияние карбоксильной группы на гидролиз эфира. Рассмотрим вначале наиболее простой пример: простейшее карбоксил-содержащее соединение, например уксусную кислоту, и простейший сложный эфир, например этилацетат. Первый эксперимент, таким образом, состоит в измерении скорости гидролиза этилацетата в воде ( или в растворе, содержащем преимущественно воду), примерно при 37 С в присутствии изменяющихся концентраций уксусной кислоты. Известно, что гидролиз сложных эфиров катализируется кислотами ( см. рис. 24.1.3), поэтому рН не должен изменяться. Простейшее решение заключается в использовании буфера уксусная кислота - ацетат натрия для сохранения постоянства рН и изменении концентрации - этого буфера. В обоих случаях результат почти всегда одинаков: ни уксусная кислота, ни ацетат-ион в заметной степени не катализируют гидролиз простого субстрата типа этилацетата. [40]
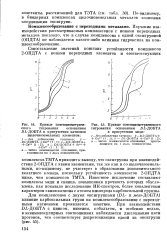 |
Кривые потенциометриче.| Кривые потенциометрического. [41] |
ТМТА приводит к выводу, что оксигруппа при взаимодействии 2 - ОПДТА с этими элементами, так же как и со щелочноземельными, по-видимому, не участвует в образовании дополнительного хелатного кольца, поскольку устойчивость комплексов 2 - ОПДТА ниже, чем комплексов ТМТА. Известное исключение составляют комплексы меди и свинца, повышенная прочность которых обусловлена, как показало исследование ИК-спектров, более ковалентным характером связи катиона с атомом кислорода карбоксильной группы. Для комплексонов с двумя оксигруппами ( DL - и леезо - ДОБТА) влияние карбоксильных групп на Комплексообразование с переходными катионами проявляется заметнее. [42]
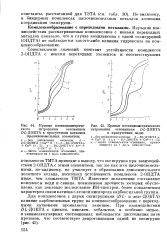 |
Кривые потенциометриче.| Кривые потенциометрического титрования основанием.. - ДОБТА. [43] |
ТМТА приводит к выводу, что оксигруппа при взаимодействии 2 - ОПДТА с этими элементами, так же как и со щелочноземельными, по-видимому, не участвует в образовании дополнительного хелатного кольца, поскольку устойчивость комплексов 2 - ОПДТА ниже, чем комплексов ТМТА. Известное исключение составляют комплексы меди и свинца, повышенная прочность которых обусловлена, как показало исследование ИК-спектров, более ковалентным характером связи катиона с атомом кислорода карбоксильной группы. Для комплексонов с двумя оксигруппами ( DL - и л езо - ДОБТА) влияние карбоксильных групп на Комплексообразование с переходными катионами проявляется заметнее. [44]
Из ненасыщенных кислот, имеющих двойную связь, удаленную от карбоксильной группы, р у-ненасыщенные кислоты ведут себя еще как акриловые кислоты, галоген стремится занять отдаленное от карбоксила положение у, § - ненасыщенныекислоты присоединяют галоген в обратном порядке: он занимает у-положение. Впрочем, соответствующие опыты проведены с веществами, имеющими относительно короткую цепь атомов углерода, а именно с пентеновыми кислотами. В случае пентен-3 - кислоты СН3СН: СНСН2СООН - - CH3 - CHJ - СН2СН2СООН можно еще говорить о влиянии карбоксильной группы, но для пентен-4 - кислоты СН2: СН-СН2СН2СООН образование СН3 - СШ-СН2СН2-СООН обусловливается не обращением влияния карбоксильной группы, а тем, что в конечной винильной группе в соответствии с приведенным выше правилом галоген присоединяется к атому углерода, более бедному водородом. [45]
Страницы: 1 2 3 4