Влияние - замещающая группа
Cтраница 2
 |
Взаимосвязь потенциалов полуволн ( а электроокисления СФТ ( рН 2 0-и констант Гаммета ( б со значениями т ПВХ-компо-звций ( 175 С. Цифры у точек соответствуют номеру СФТ в 43. [16] |
Различие в эффективности СФТ является следствием влияния замещающих групп. Заместители, обусловливающие увеличение отрицательного индуктивного эффекта, повышают стабилизирующее действие СФТ. Электроноакцепторные группы ( например, группа - СООН в - положении у 2 6-ди-т / грет-бутилфенола) понижают эффективность СФТ как стабилизаторов-антиоксидантов ПВХ. [17]
Из табл. 65 видно также, что влияние замещающих групп в случае фениловых эфиров передается в большей степени, чем в случае бензиловых, вследствие наличия в последних метиленовой группы, разрывающей сопряжение. [18]
Из табл. 68 видно также, что влияние замещающих групп в случае фениловых эфиров передается в большей степени, чем в случае Зензиловых, вследствие наличия в последних метиленовой группы, разрывающей сопряжение. [19]
Следует подчеркнуть, что подход к проблеме влияния замещающих групп в реакциях гомолитического присоединения был до настоящего времени исключительно эмпирическим. Предстоит еще большая работа, пока удастся точно оценить роль различных факторов. [20]
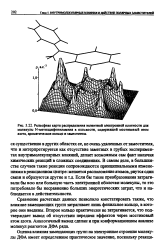 |
Рельефная карта распределения валентной электронной плотности для молекулы N-метилдифениламнна в плоскости, содержащей мостиковый атом азота, ароматическое кольцо и заместитель. [21] |
Сравнение расчетных данных позволило констатировать также, что влияние замещающих групп затрагивает лишь фенильное кольцо, в которое они введены. Второе кольцо практически не затрагивается, что подтверждает вывод об отсутствии передачи эффектов через мостиковый атом азота. Аналогичный вывод сделан и при конформационном анализе молекул реагентов ДФА ряда. [22]
 |
Каталитическое гидрирование пиррольного ядра при 30. [23] |
Противоречивость данных различных исследователей относительно легкости гидрирования и влияния замещающих групп на скорость гидрирования пирролов, вероятно, объясняется нестабильностью пирролов на воздухе, а также недостаточно тщательной очисткой исходного материала перед гидрированием и различиями условий гидрирования. [24]
Влияние различных заместителей на скорость полимеризации диолефинов аналогично влиянию замещающих групп на полимеризацию олефинов. В присутствии алкильных групп и в этом случае уменьшается реакционная способность углеводородов, а соединения, в которых содержатся две метиленовые группы, полимеризуются легче, чем соединения с одной такой группой. [25]
Дальнейшее подтверждение правильности такого предположения было получено при изучении влияния замещающих групп на скорость реакций, особенно путем изучения скорости гидролиза эфиров в присутствии щелочей, а также взаимодействия различных реагентов с производными кислот. [26]
Дальнейшее подтверждение правильности такого предположения было получено при изучении влияния замещающих групп на скорость реакций, особенно путем изучения скорости гидролиза эфирен в присутствии щелочей, а также взаимодействия различных реаген тов с производными кислот. [27]
Значительный экспериментальный материал, накопленный к настоящему времени о влиянии замещающих групп на степень диссоциации замещенных этапов, позволяет на основе представлений органической химии сделать выводы о факторах, облегчающих диссоциацию на свободные радикалы, и о причинах их устойчивости. Прежде чем перейти к обсуждению этих данных, следует рассмотреть вопрос о пространственной направленности валентных связей углеродного атома, имеющего формально один неспаренный электрон. [28]
Значительный экспериментальный материал, накопленный к настоящему времени, о влиянии замещающих групп на степень диссоциации замещенных этапов позволяет на основе представлений органической химии сделать выводы о факторах, облегчающих диссоциацию на свободные радикалы, и о причинах их устойчивости. Прежде чем перейти к обсуждению этих данных, следует рассмотреть вопрос о пространственной направленности валентных связей углеродного атома, имеющего формально один неспаренный электрон. [29]
Из этих таблиц видно, что скорость реакции изменяется в соответствии с влиянием замещающих групп на величину положительного заряда углерода группы СО. При сопоставлении данных табл. 65 для щелочного гидролиза эфиров замещенных бензилового спирта и фенола видно, что во всех случаях гидролиз фениловых эфиров протекает быстрее, чем бензиловых. [30]
Страницы: 1 2 3 4