Структура - белок
Cтраница 1
Структура белка может быть значительно старше, чем его функция. Лактальбумин, например, который появился как функциональная составляющая молочных желез около 100 миллионов лет назад, существовал, вероятно, в виде лизоцимподобного белка задолго до того, как возникла потребность в этой функции. По-видимому любая термодинамически возможная функция может развиться на основе существующих белковых структур ( ср. [1]
Структура белка инсулина, а также некоторых природных полипептидов ( с более низким молекулярным весом) однозначно установлена химическим синтезом этих соединений. [2]
Подробнее структура белков определяется анализом частичных гидро-лизатов, полученных либо кислотным, либо ферментативным гидролизом. При этом выделяют отдельные пептиды, образовавшиеся при расщеплении белков, и в них определяют последовательность аминокислот. Применяя различные виды гидролиза, мытом самым стремимся обнаружить пептидные осколки, в которых аминокислоты взаимно перекрывали бы друг друга. Например, последовательность чередования аминокислот в пептидах, которые содержат аминокислоты A, JJ, (, D, Е и /, можно установить, если мы обнаружим пептиды Л - В - С nD - E-F, а также еще не менее одного пептида, например C-D, который обусловливает непрерывность в пептидной цепочке ( см. стр. [3]
Такая структура белка называется вторичной. [4]
Анализ структуры белка является первым этапом в исследованиях механизма его действия и в конечном счете его биологической функции. В настоящее время наиболее хорошо изучены функции гемоглобина и химотрипсина. [5]
Обсуждение структуры белка облегчается тем, что мы можем рассматривать четыре различных структурных уровня: первичный, вторичный, третичный и четвертичный. Первичной структурой называют последовательность аминокислот в полипептидной цепи, как, например, на рис. 40.1. Вторичная структура - - это способ расположения полипептидной цепи в пространстве. Вторичная структура определяется поступательными и вращательными движениями составляющих пептидной цепи и водородными связями между компонентами пептидной цепи. Полная структура полипептида предполагает трехмерную кон-формацию. Третичная структура - это и есть обозначение такой полной конформации, а также взаимодействий, которыми она обусловлена. Четвертичная структура обусловлена ассоциацией двух или более полипептидных цепей. Исследования биохимии белков показывают, что именно таким образом построено большинство биологически важных белков. [6]
Изучению структуры белков рибонуклеиновых ( РНК) и дезокси-рибонуклеиновых ( ДНК) кислот - в настоящее время уделяется исключительно большое внимание не только в биологии, но и в математике, физике и материаловедении в связи с программой создания наност-руктурных материалов и технологий их получения. К настоящему времени достигнуты фантастические успехи в молекулярной биологии по изучению генов различных белков, приведшие к клонированию и регуляции активности белков. [7]
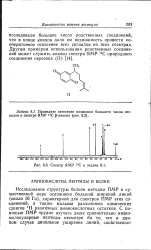 |
Спектр ЯМР 13С к задаче. [8] |
Исследование структуры белков методом ПМР в существенной мере осложнено большой шириной линий ( около 10 Гц), характерной для спектров ПМР этих соединений, а также малыми различиями химических сдвигов Н различных аминокислотных остатков. [9]
Изменение структуры белков в процессах денатурации обычно связано с К. [10]
Обсуждение структуры белка облегчается тем, что мы можем рассматривать четыре различных структурных уровня: первичный, вторичный, третичный и четвертичный. Первичной структурой называют последовательность аминокислот в полипептидной цепи, как, например, на рис. 40.1. Вторичная структура - это способ расположения полипептидной цепи в пространстве. Вторичная структура определяется поступательными и вращательными движениями составляющих пептидной цепи и водородными связями между компонентами пептидной цепи. Полная структура полипептида предполагает трехмерную кон-формацию. Третичная структура - это и есть обозначение такой полной конформации, а также взаимодействий, которыми она обусловлена. Четвертичная структура обусловлена ассоциацией двух или более полипептидных цепей. Исследования биохимии белков показывают, что именно таким образом построено большинство биологически важных белков. [11]
Изучение структуры белка не позволяет объяснить причину такого превосходства ферментов над катализаторами, изготовленными современной химией. [12]
Детали структуры белка и ультраструктуры фитохрома полностью не установлены; структура белка у разных видов растений, по-видимому, различна. Тетрапиррольный хромофор, который может быть выделен (5.44), оказался сходным с фикобилинами водорослей. Точно характер связи хромофора с белком еще не известен, но ясно, что эта связь отличается от той, которая имеется у фикобилипротеинов. На рис. 5.16 показаны предполагаемое связывание тетрапиррол - белок у Рг-формы фитохрома и механизм ее превращения в Pfr-форму. [13]
Изменение структуры белков в процессах денатурации обычно связано с К. [14]
Анализ структуры белка является первым этапом в исследованиях механизма его действия и в конечном счете его биологической функции. В настоящее время наиболее хорошо изучены функции гемоглобина и химотрипсина. [15]
Страницы: 1 2 3 4