Электронное влияние - заместитель
Cтраница 1
Электронное влияние заместителей на нуклеофильность аналогично их влиянию на основность тех же нуклеофилов при неизменности реакционного центра. Электроотрицательные и - - заместители уменьшают нуклеофильность и увеличивают электроотрицательность уходящей группы. Кроме этого, объемистые заместители обусловливают появление стерических препятствий, уменьшающих нуклеофильность. [1]
Электронное влияние заместителя R в значительной мере определяет стабильность енгидразина. [2]
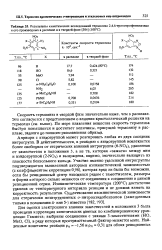 |
Результаты кинетических исследований термолиза 2 4 6-тринитрофенилазида и его производных в расплаве и в твердой фазе ( 100 С. [3] |
Для оценки электронного влияния заместителей в положении 3 была проведена корреляция кинетических данных по комбинированному уравнению Гаммета; выбраны соединения с такими 3-заместителями НО, MeO, C1), в ряду которых пространственный фактор меняется мало. [4]
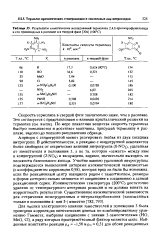 |
Результаты кинетических исследований термолиза 2 4 6-тринитрофеннлазнда и его производных в расплаве и в твердой фазе ( 100 С. [5] |
Для оценки электронного влияния заместителей в положении 3 была проведена корреляция кинетических данных по комбинированному уравнению Гаммета; выбраны соединения с такими 3-заместителями НО, MeO, CI), в ряду которых пространственный фактор меняется мало. [6]
Независимо от электронных влияний заместителей, моно - и 1 1-дизамещенные этилены всегда взаимодействуют с нитронами с образованием 5-замещенных изоксазолидинов. [7]
Условия передачи электронного влияния заместителя X на реакционный центр также влияют на абсолютное значение константы реакции. [8]
Реакция проходит благодаря электронным влияниям заместителя у азота, что подтверждается стабильностью в применяемых условиях N-ацетильного производного. [9]
Удобными моделями для изучения электронных влияний заместителей, находящихся у тройной связи, на реакционную способность последней являются ара-замещенные аминоспирты фенилацетиленово-го ряда, так как наличие фенильного кольца между тройной связью и варьируемым заместителем позволяет исключить маскирующие сте-рические эффекты. По сравнению с алкильными заместителями фенилъ-ная группа является заместителем, несколько активирующим тройную связь. [10]
Как уже указывалось выше, электронное влияние триалкилсилиль-ных заместителей на тройную связь является суммой двух эффектов - - положительного индуктивного и эффекта ( р - ( взаимодействия, причем каждый из них в отдельности может затруднять нуклеофильную атаку азота по первому углеродному атому кремниизамещенной тройной связи. Для оценки влияния каждого из этих двух эффектов на реакционную способность тройной связи в рассматриваемой реакции была изучена циклизация кремнийацетиленовых 5-аминоспиртов, в которых между атоиом кремния и тройной связью введена в одном случае метиленовая, а в другом - фенильная группы. [11]
В работах [104, 105] выявлены закономерности электронного влияния заместителей на течение фотонзомеризацнн. [12]
Величина такого спектрального сдвига должна отражать электронное влияние заместителей. [13]
При присоединении Дильса - Альдера хорошо изучено электронное влияние заместителя. Для реакций с большинством диепов наиболее пригодны алкены, которые содержат электроноакцепчлрпые зруппы. Так, к наиболее реагадиои неспособным дненофилам относятся хнноны, малев-новый ангидрид и нитроалкены. Эффективными диенофиламн являются также х, 3-ненасыщешше сложные эфлры, кетоиы и нитрилы, Важно отметить, что при использовании улемронодефицитцых диенов предпочтительно применять богатые электронами диенофилы; это значит, что полярность переходного состояния становится обратной. [14]
При присоединении Дильса - Альдера хорошо изучено электронное влияние заместителя. Для реакций с большинством диенов наиболее пригодны алкены, которые содержат электроне акцепторные труппы. Таку к наиболее реакциоиноспособным дленофил-ам относятся хиноиы, малеи-новый ангидрид и нитроалкеиы. Эффективными диеаофилзми являются также аг ( 3-ненасыщешше сложные эфлры, кетоиы н нитрилы, Важно отметить, что при использовании электр оно дефицитных диенов предпочтительно применять богатые электронами диенофилы; это значит, что нолярность переходного состояния становится обратной. Например, реакция гексахлорциклопегетадиена со стиролами ускоряется при наличии в молекуле стирола электронедонорных. [15]
Страницы: 1 2 3 4