Электронное влияние - заместитель
Cтраница 2
При присоединении Дильса - Альдера хорошо изучено электронное влияние заместителя. Для реакций с большинством диепов наиболее пригодны элкены, которые содержат электроноакцепшрпые группы. Так, к наиболее реакциошчоспособньш дненофилам относятся хинотгы. Эффективными диеаофилзмн являются также а р-ненасыщешше сложные эфлры, кетоиы и нитрилы, Важно отметить, что при использовании улемронодефицитцых диенов предпочтительно применять богатые электронами диенофилы; это значит, что полярность переходного состояния становится обратной. [16]
Рассмотрим на примере анилина, каким образом электронные влияния заместителя передаются преимущественно в орто - и пара-положения. Аминогруппа проявляет в основном М - эффект: это значит, что электронная плотность свободной электронной пары азота частично смещается к ароматическому ядру. [17]
Дальнейшим подтверждением высказанной точки зрении на механизм электронных влияний заместителей с неподеленной парой электронов в я-сопряжении могут служить данные по смещениям Ямакс в карбанионах 6 - ОСНз, 6 - С1, 6 - F-2 - метил-хинолинов. Однако наблюдаемые Ямакс в спектрах гетероциклических карбанионов с теми же заместителями отклоняются от такой последовательности ( РОСНзСН3С1), что может быть отнесено только за счет участия / л - эффекта. [18]
Таким образом, циклопропановое кольцо более эффективно передает электронное влияние заместителей. [19]
Коэффициент р характеризует чувствительность данной серии реакций к электронному влиянию заместителей относительно реакции, принятой за стандарт. Чем выше р, тем больше выражено это влияние. [20]
В случае соединений II-V различная легкость расщепления зависит от электронного влияния заместителей, связанных с карбонильной группой. Так, мезомерный эффект уменьшается при переходе от атома азота ( II) к атому кислорода ( III) и затем к атому углерода ( IV), и основность карбонильной группы возрастает в ряду эфиров бензойной, угольной, карбамино-вой и ксантогеиовой кислот. В случае ацетата ( V) на карбонильный кислород оказывает действие лишь сравнительно слабый индуктивный эффект ( /) метильной группы. [21]
Так как скорость кислотного гидролиза слабо чувствительна к изменению электронного влияния заместителя и сильно чувствительна к стерическому влиянию, Тафтом было предложено использовать процесс кислотного гидролиза этиловых эфиров алифатических кислот для определения стерических констант заместителей. [22]
Проведенный таким образом квантовохимический анализ подтверждает преимущественно индукционный механизм электронного влияния заместителей как на химический сдвиг протонов, так и на химический сдвиг углерода алкильной группы в исследованной серии производных метана и сходных с ними соединений. [23]
Так как скорость кислотного гидролиза слабо чувствительна к изменению электронного влияния заместителя и сильно чувствительна к стерическому влиянию, Тафт предложил использовать процесс кислотного гидролиза этиловых эфиров алифатических кислот для определения стерпческих констант заместителей. [24]
СО-групп, что, вероятно, связано с передачей электронного влияния заместителей при атоме германия через связь Ge-Мп на распределение электронов связи С-О. В ИК-спектре соединения XI имеется интенсивная полоса при 865 см-1, соответствующая связи Ge-О - Ge, и отсутствует поглощение в области 2000 см-1, характерное для СО-групп. [25]
Как уже говорилось, р отражает чувствительность процесса к электронному влиянию заместителя. Если реакционный параметр имеет положительный знак, это свидетельствует о том, что константа скорости или равновесия реакции увеличивается при введении электроноакцепторных заместителей. Отрицательное значение реакционного параметра соответствует увеличению скорости реакции при введении электронодонорных заместителей. [26]
Как уже говорилось, п отражает чувствительность процесса к электронному влиянию заместителя. Если реакционный параметр имеет положительный знак, эю свидетельствует о том. Отрицательное значение реакционного параметра соответствует увеличению скорости реакции при введении электронодонорных заместителей. [27]
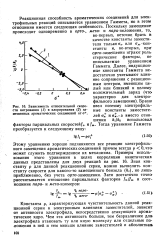 |
Зависимость относительной скорости нитрования ( / и хлорирования ( 2 замещенных ароматических соединений от ч. [28] |
Константа р, характеризующая чувствительность данной реакционной серии к электронным влияниям заместителей, зависит от активности электрофила, непосредственно атакующего ароматическое ядро. [29]
На скорости полимеризации сказываются и стерические и, особенно, электронные влияния заместителей у кремния. Она увеличивается при замещении метальных групп в Д3 и Д4 электро-ноакцепторнъши группами, облегчающими нуклеофильную атаку активным центром атомов кремния в цикле благодаря повышению их дробного положительного заряда. Слабее влияют 3 3 3-трифторпропильные группы ( скорости возрастают в 3 - 4 раза при переходе от Д3 к Ф3 и от Д4 к Ф4) [33, 40], что связано, вероятно, с противоположным действием сильных отрицательного индуктивного и стерического эффектов этих групп. [30]
Страницы: 1 2 3 4