Индукционное влияние - заместитель
Cтраница 2
 |
Зависимость g k для реакций. [16] |
Последние были получены [730] и свидетельствуют о том, что в рассматриваемой реакции имеет место также небольшое индукционное влияние заместителя R. В результате и эта реакция не годится для определения чисто стерических постоянных. [17]
Таким образом, различие в скоростях реакций кислотного и щелочного гидролиза эфиров обусловлено исключительно различиями в индукционном влиянии заместителей в этих реакциях, точнее различиями / - эффектов заместителей в соответствующих переходных состояниях. [18]
IIIVI, III, причем определяющее влияние оказывает индукционный эффект ближайшего моста MI и, в меньшей степени, сказывается индукционное влияние заместителя. Дальний мост М2 на реакционную способность не влияет. [19]
Это подтверждается и корреляцией батохром-ного смещения р - полосы поглощения системы А стп константами заместителей по значению я ш для серии V, где учитывается и индукционное влияние заместителей. Выход системы из сопряжения в этом случае возможен тогда, когда при возбуждении молекул в спектре хромофорной системы А имеется значительное разделение зарядов, по типу хиноидного и ионоидного состояния, а влияние заместителей приводит к увеличению диэдрального угла в производных бифенила и дифени-локсида. [20]
Это подтверждается и корреляцией батохром-ного смещения / / - полосы поглощения системы А ап константами заместителей по значению л ш для серии V, где учитывается и индукционное влияние заместителей. Выход системы из сопряжения в этом случае возможен тогда, когда при возбуждении молекул в спектре хромофорной системы А имеется значительное разделение зарядов, по типу хиноидного и ионоидного состояния, а влияние заместителей приводит к увеличению диэдрального угла в производных бифенила и дифени-локсида. [21]
Аналогичный эффект изменения характера влияния заместителей может быть вызван изменением степени ионизации разрывающейся связи, вплоть до ее полной ионизации в ионной паре, в результате изменения индукционного влияния заместителя. [22]
В рамках этой модели незначительные батохромные сдвиги, наблюдаемые в алкилзамещенных альтернантных углеводородах, вызваны гиперконъюгацией, в то время как в неальтернант-ном ряду сдвиги в основном обусловлены индукционными влияниями заместителей, подавляющими вызванный гиперконъюгацией небольшой батохромный сдвиг. [23]
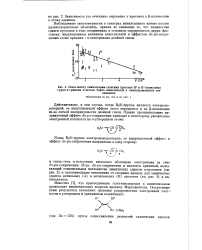 |
Связь между химическими сдвигами протонов Н1 и Н3 винильных групп и суммами констант Тафта заместителей в винилкремниевых сое. [24] |
Наблюдаемые закономерности в спектрах винилсиланов можно вполне удовлетворительно объяснить, приняв во внимание то, что химические сдвиги протонов в этих соединениях в основном определяются двумя факторами: индукционным влиянием заместителей и эффектом Ат-ря-сопря - жения атома кремния с я-электронами двойной связи. [25]
Индукционное влияние заместителей на силу оснований аналогично наблюдаемому в вытперассмотренных примерах для кислот. Заместители в основаниях типа XtX XgK связаны непосредственно с протоноакцепторным атомом, обладающим свободной электронной парой. Таким образом, они оказывают непосредственное влияние и вместе с другими эффектами существенно влияют на силу основания. [26]
 |
Константы гидролиза некоторых 2 4-дихлорпроизводных. [27] |
Следовательно, хлор - и 0-алкил-гидроксиламиновые производные смлш-триазина характеризуются большей реакционной способностью в щелочном гидролизе, чем соответствующие алкиламино-производные. Передача индукционного влияния заместителей через триазиновое кольцо может быть описана уравнением Гаммета. Применимость этого уравнения к соединениям триазинового ряда подтверждена [140] на примере кислотного гидролиза, проводимого в интервале содержаний H2SO4 от 0 01 до 12 % в среде этиленгликоля и воды при 70 С. [28]
Расстояние между отрицательно заряженными атомами кислорода карбоксилатной группы и положительно заряженным атомом азота в N02 или М ( СН3) з равно 6 50 А, а эффективное расстояние между этими же атомами кислорода и атомами кислорода нитро-группы равно 7 45 А. Иными словами, в этом плане индукционное влияние заместителей через алициклический фрагмент не отличается от такового в чисто алифатических системах. [29]
Эффективные методы разделения смесей терпенофенолов основаны на различиях в способности изомеров ( I-III) к образованию фенолятов и в их адсорбционных и сорбционных свойствах. Эти различия связаны главным образом с суммарными стерическими и индукционными влияниями различно расположенных заместителей на свойства фенольного гидроксила. Для оценки этих различий служат величины констант диссоциации, значения Rf при хроматографировании в тонком слое и относительное время удерживания при газо-жидкостной хроматографии. [30]
Страницы: 1 2 3 4