Индукционное влияние - заместитель
Cтраница 3
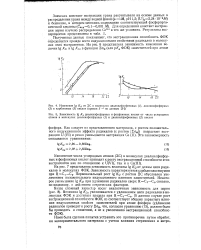
На рис. 7 представлена зависимость величины lg / Си от длины цепи радикалов в молекулах ФОК. Первоначальный рост lg / Си с ростом 2С обусловлен увеличением положительного индукционного влияния заместителей. Некоторое уменьшение lg / Си при удлинении радикалов сверх RC - C9 связано, по-видимому, с действием сгерических факторов. [32]
Более того, молекула, обладающая структурой 149, находясь в виде г мс-изомера ( ifuc - арил - или г ие-карбэтокси -), должна быть пространственно более напряженной, чем торакс-изомер. Замещение р-водородного атома цианогруппой увеличивает скорость расщепления [301], по-видимому, благодаря индукционному влиянию заместителя. Резонансный эффект цианогруппы приводит к увеличению электрофильности a - углеродного атома и общему повышению реакционной способности. [33]
Более того, молекула, обладающая структурой 149, находясь в виде цие-изомера ( i uc - арил - или ifue - карбэтокси -), должна быть пространственно более напряженной, чем теракс-изомер. Замещение ( 3-водородного атома цианогруппой увеличивает скорость расщепления [301], по-видимому, благодаря индукционному влиянию заместителя. Резонансный эффект цианогруппы приводит к увеличению электрофильности ос-углеродного атома и общему повышению реакционной способности. [34]
Это говорит о принципиальном различии в механизме. Если реакция (3.1) является электрофильным присоединением, то реакция (3.3) - нуклеофильным, и поэтому индукционное влияние заместителей имеет обратный знак. [35]
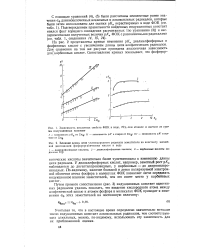
У диалкилфосфорных кислот, например, заметный рост р / С0 наблюдается до дигептилпроизводных, у карбоновых - до дипропилпро-изводных. По-видимому, наличие большой и легко поляризуемой электронной оболочки атома фосфора в молекулах ФОК позволяет легче передавать индукционное влияние заместителей, чем это имеет место у карбоновых кис / ют. [37]
При обработке экспериментальных величин 0 согласно этим уравнениям прежде всего встает вопрос о значениях используемых индукционных и резонансных постоянных. В случае индукционных параметров у нас имеется некоторая предварительная уверенность, поскольку величины о оказались применимыми для описания индукционного влияния заместителей через али-циклические системы. В случае резонансных постоянных мы располагаем только величинами а. [38]
Исключение составляет лишь модель электростатического взаимодействия между ионными заместителями, рассмотренная в разделе III. Однако учет такого характерного для заряженных заместителей взаимодействия вряд ли имеет отношение к самому индукционному эффекту, если аналогичный подход к индукционному влиянию электронейтральных заместителей ( или взаимодействию между заряженными и электронейтральными заместителями) оказывается невозможным, а полный эффект заряженных заместителей не исчерпывается электростатическим взаимодействием между ними. [39]
Переход от спиртов ROH к гидропероксидам ROOH приводит к увеличению кислотных свойств Н - О-группы. При этом сопоставление двух корреляционных уравнений для кислотности RCH2OH и ROOH, по данным работ [42,43], позволяет определить для О-мостика в гидропер-оксидной группе относительную величину трансмиссионного фактора Ф, характеризующего способность кислородного атома передавать индукционное влияние заместителя R на свойства Н - О-группы по сравнению с СН2 - группой. [40]
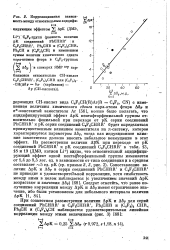 |
Корреляционная зависимость между относительным ацидифи. [41] |
Абр и а - константой заместителя Аг [56], можно было полагать, что ацидифицирующий эффект АрК пентафторфенильной группы относительно фенильной при переходе от рК серии соединений PhCHRR к рК серии соединений C6F5CHRR будет определяться преимущественным влиянием заместителя на я-систему, которое характеризуется параметром Абр, тогда как индукционное влияние заместителя должно вносить небольшое возмущение в этот эффект. Из рассмотрения величин ДрК при переходе от рК соединений PhCHRR к рК соединений C6F5CHRR в табл. 13; 18 и 19 ( ДМЭ, катион Li) видно, что относительный ацидифицирующий эффект одной пентафторфенильной группы изменяется от 1 4 до 9 5 лог. [42]
Как следует из рисунка, между этими величинами не наблюдается удовлетворительной корреляции. Отсюда можно сделать вывод, что кроме чисто индукционного влияния заместителя большое значение имеют другие ( по-видимому, главным образом, стерические) факторы. [43]
На рис. 1 представлена зависимость lg К от индукционной константы а Тафта при 20 С. Как следует из рисунка, между этими величинами не наблюдается удовлетворительной корреляции. Отсюда можно сделать вывод, что кроме чисто индукционного влияния заместителя большое значение имеют другие ( по-видимому, главным образом, стерические) факторы. [44]
Вторым механизмом влияния среды является донорно-ак-цепторное взаимодействие. Заместители, в которых один из атомов обеднен электронами или имеет частично незаполненные орбиты, вступают в такое взаимодействие в качестве акцепторов. Этот сдвиг, отвечающий увеличению экранирования, указывает на ослабление индукционного влияния заместителя на бензольное кольцо. [45]
Страницы: 1 2 3 4