Изокинетическая температура
Cтраница 1
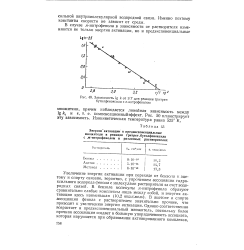 |
Зависимость lg k от / Т для реакции тритрет-бутилфеноксила с о-нитрофенолом. [1] |
Изокинетическая температура равна 525 К. [2]
Изокинетическая температура, как легко видеть, является более важной характеристикой реакции, чем, например, константа р, которая, по существу, позволяет оценить скорость изменения влияния заместителей в зависимости от изменения температуры. [3]
Близость изокинетической температуры в случае этой реакционной серии ощущается весьма наглядно, поскольку в исследованном интервале температур величина р уменьшается по мере роста температуры в два раза. [4]
 |
Частные случаи эмпирической зависимости А / / А - г. [5] |
При изокинетической температуре все / реакций серии q идут с одинаковой скоростью. Причина этого состоит в том, что нормальная реакция, которая приводит к образованию активного комплекса А, при изокинетической температуре для всех / однотипных реакций серии q протекает обратимо. [6]
При изокинетической температуре все AG - 0; константы скорости всех реакций вида q должны были бы быть одинаковыми и равными KinekbT / h, если при Т - В в данной системе реакции вида q могли бы протекать. [7]
Согласно данным этих таблиц, изокинетическая температура будет больше экспериментальной только в том случае, если затрагиваются очень высокие занятые уровни. Интересно, что возможно существование отрицательных изокинетических температур, но эти случаи редки и реализуются лишь при условии, что действительные изменения энтальпии и энтропии невелики. [8]
Для отрицательных значений В термин изокинетическая температура теряет смысл, так как температура по определению положительна. Физические причины отрицательных значений параметра В могут быть следующими. [9]
Возможно, что и семейство изокинетических температур следует рассматривать не как константу, а как функцию экспериментальной температуры. Несмотря на это, Леффлер и Грюнвальд [136] считали изменения теплоемкости неощутимо малыми. По-видимому, их доводы верны при изучении реакционной способности соединений небольшой полярности, однако в таких случаях мы и не ожидали большой чувствительности к действию заместителей и, следовательно, хорошей корреляции с помощью уравнений ЛСЭ. [10]
В остальных известных случаях переход через изокинетическую температуру сопровождается обращением знака эффектов заместителей или растворителя. [11]
При обобщении этих особенностей утверждалось, что все отрицательные изокинетические температуры связаны с эффективными константами, подобными рассмотренным выше. Такая точка зрения подтверждается, если принять во внимание, что все известные из литературы примеры антикомпенсации укладываются в эту схему. Известно; что в случае реакций в растворах с участием заряженных частиц эффекты сольватации часто оказывают доминирующее влияние как на энтропию реакции, так и на энтропию активации. Поэтому можно предсказать, что оттягивание электронов от реакционного центра должно приводить к уменьшению АЯ абл и к менее отрицательной А5 абл. [12]
Наибольшее принципиальное значение имееет вопрос об экспериментальной достижимости изокинетической температуры и других изопараметрических точек. Если бы они были экспериментально недостижимы, то ИЗ и другие изопараметрические зависимости представляли бы ограниченный интерес. [13]
А и Е выполняется приближенно, то при изокинетической температуре различия между константами скорости реакций взятого ряда минимальны. [14]
Предполагается, что сравниваемые реакции характеризуются одинаково высокими значениями изокинетической температуры. [15]
Страницы: 1 2 3 4