Изокинетическая температура
Cтраница 2
Только в одном случае сообщается о своеобразном нарушении ИЗ при изокинетической температуре. Автором указанной работы обнаружено соблюдение двух разных ИЗ, одно из которых имеет силу при температуре ниже, а другое-выше изокинетической. При изокинетической температуре заместители действительно перестают влиять на скорость реакции ( р 0), однако при переходе через изокинетическую температуру знак р не обращается. Кроме того, очень трудно ответить на вопрос, каким образом реакция для каждого из исследованных соединений, взятая в отдельности, чувствует изокинетическую температуру, чтобы в этой точке резко изменилась энергия активации. Такое резкое изменение энергии активации обычно связывают с изменением ее механизма. [16]
В свете приведенной гипотезы становится также понятным § отсутствие единого универсального значения изокинетической температуры [ или величины у из ( IV. Дело в том, что в случае всех электронных влияний у 0 ( изоэнтропийность), и только наложение влияния водородной связи не позволяет нам о во многих случаях обнаруживать этот факт. Большое же разнообразие величин р, найденное при обработке экспериментальных данных, также находит объяснение с единой точки зрения и, что особо важно, без вступления в конфликт с приложимостью ППЛ или ЛСЭ. [17]
Таким образом, остается вопрос, касающийся не самого по себе физического смысла изокинетической температуры, а ее численного значения. Иными словами, ясно, что при Гизо вклад энтропии компенсирует вклад энтальпии, но почему это происходит только при той или иной температуре. Так, возвращаясь к примеру I, естественно спросить, почему Ni ( II) теряет способность различать некоторые лиганды при 120 С в ДМСО, но при 65 С в ацетонитриле. Ответ на подобные вопросы все еще остается задачей будущих теорий. В самом общем виде можно утверждать, что чем выше Гизо, тем в большей степени природа наблюдаемого эффекта связана с электронными явлениями, а чем ниже Гизо, тем больше роль стерических факторов. Недавно было показано [72], что чем выше изокинетическая температура, тем больше средняя высота потенциального барьера реакций данной серии и тем меньше число участвующих в процессе степеней свободы. Это должно означать, что Гизо является мерой средней энергии, сохраняемой каждой степенью свободы при распределении по степеням свободы в активированном состоянии. [18]
Вообще говоря при выполнении изокинетического отношения это может указывать на близость изученного температурного интервала к изокинетической температуре, величина которой в действительности является сложной функцией ряда параметров. [19]
Поэтому естественно желание исследовать, действительно ли возможно построить общую модель, из которой следует, что изокинетическая температура больше экспериментальной. [20]
Здесь Л 0, Е0 - предэкспонент и энергия активации эталонного катализатора, a Ts, у - изокинетическая температура и эмпирическая постоянная для данной серии катализаторов. Очевидно, что применение уравнения (V.25) требует достаточно большой предварительной экспериментальной работы, чтобы определить параметры А0, Ts, E0, у одним из стандартных статистических методов по данным для нескольких катализаторов серии. Однако после этого имеется широкая возможность расчетной оценки различных катализаторов данного вида как априорной, так и по данным только физико-химических определений. На рис. V.9 приведены сравнения расчетных и экспериментальных данных по катализаторам изомеризации о - и л-ксилолов. [21]
Его применение, хотя и трудоемкое, абсолютно необходимо для того, чтобы установить изокинетиче-ское соотношение и определить изокинетическую температуру. Этим методом были рассмотрены все приведенные ниже экспериментальные примеры. [22]
В точке пересечения двух аррениусовских прямых k - ka и, следовательно, солевой эффект отсутствует, что соответствует изокинетической температуре для солевого эффекта. [23]
Указанные авторы показали, что одни лишь эти экспериментальные ошибки могут являться причиной кажущегося соблюдения ИЗ с наклоном 0 ( изокинетической температурой), равным средней температуре эксперимента, если даже величина константы k скорости или равновесия остается постоянной в пределах всей рассматриваемой реакционной серии. В связи с этим наклон 3, равный или близкий средней температуре эксперимента, получил название ошибочного наклона. В случаях, если постоянство k в пределах данной реакционной серии не имеет места, ошибочный наклон определяет направление максимального возмущения, вызываемого экспериментальными ошибками. Наложение этого возмущения приводит к тому, что наблюдаемое значение 3 отклоняется от истинной изокинетической температуры в сторону средней температуры эксперимента. [24]
Зависимость ДЯ от Д5 для различных растворителей хорошо укладывается на прямую, что указывает на существование здесь эффекта компенсации с изокинетической температурой - 9 С. Авторы [35] объясняют такую зависимость влиянием диэлектрической постоянной среды на диполь-дипольное взаимодействие двух диспро-порционирующих радикалов в активированном комплексе. [25]
В таком случае мы не можем сказать, является ли данная реакционная серия изоэнтропийной, изоэнтальпийной или характеризуется любым отрицательным значением изокинетической температуры. [26]
Иногда изокинетическое отношение справедливо для серии реакций, проведенных при варьировании среды; тогда, если протеканию реакции способствуют неполярные растворители, то выше изокинетической температуры реакция будет идти быстрее в полярных растворителях. Такое явление кажется парадоксальным, так как механизм реакции остается прежним, но оно является следствием компенсационного эффекта в изменениях энтальпии и энтропии активации. [27]
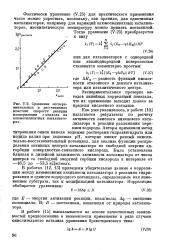 |
Сравнение экспериментальных и рассчитанных констант скорости реакции изомеризации о-ксилола на алюмосиликатных катализаторах. [28] |
Фактически уравнение (V.25) для практического применения часто можно упростить, поскольку, как правило, для однотипных катализаторов, например для вариаций алюмосиликатных катализаторов, изокинетическую температуру можно принять постоянной. [29]
Другой набор данных соответствует гипотетической реакции, для которой прямые lg k - l / Т заведомо не пересекаются в одной точке, что равносильно отсутствию единой изокинетической температуры. Далее Петерсон [605] отмечает, что из литературы ему не известно ни одного примера, когда требование пересечения указанных прямых в одной точке соблюдалось хотя бы приближенно. [30]
Страницы: 1 2 3 4