Триптофан
Cтраница 1
Триптофан при кислотном гидролизе распадается полностью; глутамин и аспара-гин превращаются в соответствующие аминокислоты. Для получения триптофана и указанных амидов проводят полный ферментативный гидролиз смесью папаина, лейцицаминопептидазы и карбоксипептидазы. [1]
Триптофан находится почти во всех белках и часто присутствует в растениях в свободном состоянии. В отличие от других аминокислот триптофан распадается при кислотном гидролизе белков, поэтому для определения триптофана гидролиз белков проводят обычно с применением щелочи или определяют его содержание без предварительного гидролиза белков. [2]
 |
Биосинтез флавоноидсв. [3] |
Триптофан дает начало другой группе алкалоидов, известных под названием индольных алкалоидов, примерами которых могут служить эрготамин и другие производные лизер-гиновой кислоты. [4]
Триптофан является, в частности, источником образования в организме серотонина. [5]
Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. [6]
Триптофан ( ( З - индолил-сс-аминопропионовая кислота) - одна из важнейших гетероциклических аминокислот, образующихся при гидролизе белков. [7]
Триптофан имеет самую объемную боковую цепь. [8]
Триптофан разрушается при гидролизе соляной кислотой. Первичные амины могут выходить из колонки с некоторыми аминокислотами. Это может приводить к неправильным результатам количественного анализа. Перечень обнаруживаемых веществ будет сокращен всеми пептидами, которые тоже будут гидролизованы. [9]
Триптофан применяется в биохимии, микробиологии, медицинской промышленности, сельском хозяйстве. [10]
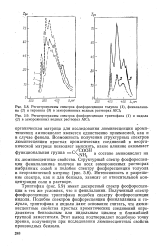
Триптофан ( рис. 5.9) имеет дискретный спектр фосфоресценции в тех же условиях, что и фенилаланин. Полученный спектр фосфоресценции триптофана подобен спектру фосфоресценции индола. Подобие спектров фосфоресценции фенилаланина и толуола, триптофана и индола дают основание считать, что люминесцентные свойства простых ароматических соединений определяются бензольным или индольным циклом и ближайшей группой заместителя. Этот вывод подтверждает подобную точку зрения, полученную при исследовании люминесцентных свойств производных бензола. [12]
Триптофан входит в состав многих белков, но обычно лишь в незначительных количествах. Определение его облегчается применением различных цветных реакций, характерных для этой аминокислоты. При кислом гидролизе протеинов он разлагается, но при ферментативном расщеплении белка может быть выделен в левовращающей форме. [13]
Триптофан содержится во многих растительных и животных белках, а также в некоторых пептидных гормонах, например в АКДТ, а - и ( 3 - МСГ и глюкагоне, и в пептидных антибиотиках, например в тироцидине В; весьма своеобразно включен остаток триптофана в молекулу фаллоидина. Наличие индольного ядра является причиной высокой реакционной способности триптофана, и синтез триптофансодержащих пептидов часто сопровождается нежелательными побочными процессами. [14]
Триптофан, р-индолилаланин-единственная природная аминокислота, содержащая индольный цикл. Он относится к числу незаменимых аминокислот и входит в состав многих белков. [15]
Страницы: 1 2 3 4