Триптофан
Cтраница 2
Триптофан является нндолил-производным алашша - одной из облигатных аминокислот, входящих в состав белков. [16]
Триптофан и другие соединения, содержащие ядро индола, дают пурпурное или фиолетовое окрашивание с реактивом Эрлиха. Типичный реактив для опрыскивания состоит из 0 5 г н-диметиламино-бензальдегида в 100 мл 95 % - ного спирта, содержащего 2 мл концентрированной соляной кислоты. [17]
Триптофан применяется в биохимии, микробиологии, медицинской промышленности, сельском хозяйстве. [18]
Триптофан ( XVIII) из его раствора в серной кислоте осаждается сернокислой ртутью. [19]
Триптофан образуют микроорганизмы бактериального и грибного происхождения: Aerobacter aerogenes, Esche-richia coli, В. [20]
Триптофан является незаменимой аминокислотой, содержание ее, особенно в растительных белках, невелико. Но потребность в триптофане значительно меньше, чем в лизине и глутаминовой кислоте. Триптофан в небольших количествах используется в животноводстве, медицине и при различных биохимических исследованиях. Вместе с тем это очень важная аминокислота, она входит в белки и участвует в многочисленных превращениях соединений, имеющих циклическую структуру. Отсутствие этой аминокислоты или нарушение процессов синтеза ее ведет к тяжелым заболеваниям организма. [21]
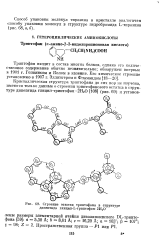 |
Строение остатка триптофана в структуре дипептида глицил - Ь - триптофан 2Н2О. [22] |
Триптофан входит в состав многих белков, однако его количественное содержание обычно незначительно; обнаружен впервые в 1901 г. Гопкинсом и Колом в казеине. [23]
Триптофан, даже если его содержание в белке относительно невысоко, определяет характер спектра флуоресценции последнего. Флуоресценция триптофана возбуждается в области длин волн 170 - 290 нм. Квантовый выход флуоресценции триптофана в водных нейтральных растворах составляет 0 16 - 0 18, а положение максимума спектра флуоресценции приходится на 354 нм. [24]
Триптофан содержится во многих растительных и животных белках, а также в некоторых пептидных гормонах, например в АКТГ, а - и р - МСГ и глюкагоне, и в пептидных антибиотиках, например в тироцидине В; весьма своеобразно включен остаток триптофана в молекулу фаллоидина. Наличие индольного ядра является причиной высокой реакционной способности триптофана, и синтез триптофансодержащих пептидов часто сопровождается нежелательными побочными процессами. [25]
Триптофан входит в состав многих белков и является незаменимой аминокислотой. [26]
Триптофан дает с ванилином и серной кислотой красную окраску, с я-нитробензальдегидом и серной кислотой-зеленую окраску. [27]
Триптофан, / ( -) - а-амино - - 3-индолпропионовая кислота, довольно широко распространен в белковых телах, хотя встречаются белки, или совсем его не содержащие, например, протамин, или содержащие в недостаточном количестве, например зеин. [28]
Триптофан входит в состав многих белков, но обычно лишь в незначительных количествах. Определение его облегчается применением различных цветных реакций, характерных для этой аминокислоты. При кислом гидролизе протеинов он разлагается, но при ферментативном расщеплении белка может быть выделен в левовращающей форме. [29]
Триптофан используют в медицине, а также как реагент в биохимических исследованиях; в небольших количествах он требуется для нужд животноводства. [30]
Страницы: 1 2 3 4