Газообразный тритий
Cтраница 1
Газообразный тритий получается по реакции Li6 ( я а) Т в виде чистого изотопа с удельной активностью - - 2 79 кюри / мл ( при нормальных условиях), что позволяет готовить его соединения с весьма высокой активностью. Однако значительная радиационная неустойчивость высококонцентрированных соединений трития мешает использованию его без носителя в химических и биологических работах. [1]
Газообразный тритий приблизительно в 10000 раз слабее поглощается организмом, чем Нг О. При этом следует подчеркнуть, что контрольные приборы описанного выше типа не различают обе эти формы трития. Однако поскольку газообразный тритий может легко подвергаться каталитическому окислению до значительно более опасной окиси трития, то лучше всего приписывать всю обнаруживаемую активность воде. [2]
Каталитический обмен с газообразным тритием по Вильцбаху [8] неудобен, так как сопровождается разложением вещества [9] под действием радиации. [3]
 |
Наиболее практически важные - излучатели. [4] |
Источник света с газообразным тритием представляет собой стеклянный баллон, на внутренней поверхности которого закреплен слой порошка люминофора. [5]
Насыщенная тритием вода и газообразный тритий являются первичными формами загрязнения тритием. Хотя насыщенная тритием вода имеет некоторое сходство с большей частью фильтровальной бумаги, использование фильтровальной бумаги не очень эффективно для взятия пробы насыщенной тритием воды. Наиболее чувствительные и точные методы измерения предусматривают поглощение конденсата пара насыщенной тритием воды. Поглощение водного пара, насыщенного тритием, из пробы воздуха происходит при пропускании пробы через ловушку с силико-гелиевым молекулярным ситом или при пропускании пробы через дистиллированную воду. [6]
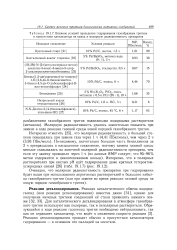 |
Влияние условий проведения гидрирования газообразным тритием в присутствии катализатора на выход и молярную радиоактивность препаратов. [7] |
Для каталитического дегалоидирования в атмосфере газообразного трития используют как полярные, так и неполярные растворители. Реакцию дегалоидирования проводят обычно в присутствии катализаторов гидрирования - в основном это палладий на носителе. [8]
Тритиевая вода была получена взаимодействием газообразного трития с окисью меди при 350 С. [9]
Особый случай взаимодействия представляет обмен почти чистого газообразного трития и органических веществ. [10]
Разработка методов получения тритированных аминокислот на основе газообразного трития, Отч. [11]
Этот метод заключается в обработке сухого вещества газообразным тритием в таких условиях, в которых происходит образование свободных радикалов. Метод не всегда пригоден для специфического введения метки. В первую очередь это ограничение относится к сахарам, которые под действием свободных радикалов образуют примесь эпимеров, обладающих высокой удельной активностью. [12]
Полученный CT3NO2 восстанавливают в солянокислый метиламин - ТБ газообразным тритием в присутствии палладия. Таким образом получают соединение, в котором водород полностью замещен тритием. [13]
Исходным для синтеза соединений, меченных тритием, является газообразный тритий или тритиевая вода. Путем гидрирования двуокиси углерода над катализатором получают тритийсодержа-щие углеводороды, из ненасыщенных углеводородов получают насыщенные, с помощью литийалюминийгидрида получают меченые спирты. Более широко используют гидратацию и гидролиз тритиевой водой. Так, гидролиз R-MgF и R - Zn - R приводит к образованию углеводородов, содержащих тритий; взаимодействие паров тритиевой воды с ацетиленом над катализатором приводит к образованию уксусного альдегида. [14]
Для извлечения трития из облученной литиевой мишени и перевода газообразного трития в Т2О наиболее пригоден следующий метод. [15]
Страницы: 1 2 3 4