Изотерма - ван-дро
Cтраница 1
Изотермы Ван-дер - Ваальса на pF - диаграмме с повышением температуры поднимаются вверх. Это сопровождается сближением объемов YI и F2 определяющих соответственно объемы жидкой и газообразной фазы. Совпадение жидкой и газообразной фазы произойдет в точке А ( см. рис. 10), которая называется критической. Эта точка определяется точкой перегиба изотермы, температура которой называется критической. [1]
Изотерма Ван-дер - Ваальса, соответствующая критической температуре Ткр вещества, имеет точку перегиба - критическую точку. [2]
Сравнение изотерм Ван-дер - Ваальса ( см. рис. 13.7) с эксперя-ментальными изотермами реальных веществ ( например, с рис. 13) показывает, что изотермы Ван-дер - Ваальса охватывают не только область газообразного состояния вещества, но также области двухфазного и жидкого состояний. Жидкому состоянию соответствуют круто уходящие вверх левые участки изотерм. Однако в этой области имеется лишь качественное согласие с результатами экспериментов. [3]
Сравнение изотерм Ван-дер - Ваальса ( рис. 12.7) с экспериментальными изотермами реальных веществ ( например, с рис. 12.5) показывает, что изотермы Ван-дер - Ваальса охватывают не только область газообразного состояния вещества, но также области двухфазного и жидкого состояний. Жидкому состоянию соответствуют круто уходящие вверх левые участки изотерм. Однако в этой области имеется лишь качественное согласие с результатами экспериментов. [4]
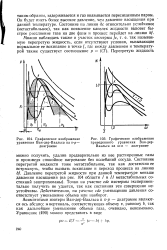 |
Графическое изображение.| Графическое изображение приведенного уравнения Ван-дер - Ваальса на ш-я - диаграмме. [5] |
Асимптотами изотерм Ван-дер - Ваальса в v - p - диаграмме являются ось абсцисс и - вертикаль, соответствующая объему v, равному Ь, так как дальнейшее уменьшение объема газа, очевидно, невозможно. [6]
У изотерм Ван-дер - Ваальса, соответствующих температурам ниже критической ( см. рис. 87.1), имеется область, в которой вещество ведет себя противоестественным образом. В этой области, простирающейся от дна впадины до вершины горба, увеличение объема сопровождается ростом давления. [7]
Среди изотерм Ван-дер - Ваальса есть такая изотерма, которая отделяет изотермы с горбами от изотерм, не имеющих горбов. [8]
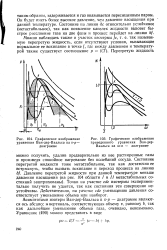 |
Графическое изображение.| Графическое изображение приведенного уравнения Ван-дер - Ваальса на ш-я - диаграмме. [9] |
Асимптотами изотерм Ван-дер - Ваальса в v - p - диаграмме являются ось абсцисс и - вертикаль, соответствующая объему v, равному Ь, так как дальнейшее уменьшение объема газа, очевидно, невозможно. [10]
У изотерм Ван-дер - Ваальса, соответствующих температурам ниже критической ( см. рис. 87.1), имеется область, в которой вещество ведет себя противоестественным образом. В этой области, простирающейся от дна впадины до вершины горба, увеличение объема сопровождается ростом давления. [11]
У изотерм Ван-дер - Ваальса, соответствующих температурам ниже критической ( см. рис. 87.1), имеется область, в которой вещество ведет себя про тивоестественным образом. В этой области, простирающейся от дна впадины до вершины горба, увеличение объема сопровождается ростом давления. [12]
Сравнивая изотерму Ван-дер - Ваальса с изотермой Эндрюса ( верхняя кривая на рис. 92), видим, что последняя имеет прямолинейный участок 2 - 6, соответствующий двухфазным состояниям вещества. Эти неустойчивые состояния называются метастабильными. Участок 2 - 3 изображает перегретую жидкость, 5 - 6 - пересыщенный пар. Обе фазы ограниченно устойчивы. [13]
Сравнивая изотерму Ван-дер - Ваальса с изотермой Эндрюса ( верхняя кривая на рис. 92), видим, что последняя имеет прямолинейный участок 2 - 6, соответствующий двухфазным состояниям вещества. [14]
Сравнивая изотерму Ван-дер - Ваальса с изотермой Эндрюса ( верхняя кривая на рис. 92), видим, что последняя имеет прямолинейный участок 2 - 6, соответствующий двухфазным состояниям вещества. Эти неустойчивые состояния называются метастабильными. Участок 2 - 3 изображает перегретую жидкость, 5 - 6 - пересыщенный пар. Обе фазы ограниченно устойчивы. [15]
Страницы: 1 2 3 4