Изотерма - ван-дро
Cтраница 2
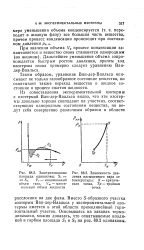
Между изотермой Ван-дер - Ваальса и опытной изотермой имеется существенное различие, как это видно из рис. 86, на котором в произвольном масштабе изображены: сплошной линией - характерный вид опытной изотермы, пунктиром - изотерма Ван-дер - Ваальса. [16]
При разборе изотерм Ван-дер - Ваальса мы видели, что при температуре выше критической они идут плавно, что не позволяет при этом различать две фазы - газообразную и жидкую. Однако твердое состояние оказывается возможным и при температуре выше критической. [17]
Участок в-г изотермы Ван-дер - Ваальса соответствует абсолютно неустойчивому состоянию вещества, которое никогда не реализуется на практике. [18]
Из сопоставления изотермы Ван-дер - Ваальса с реальной изотермой вытекает, что эти изотермы примерно совпадают на участках, отвечающих однофазным состояниям вещества, но ведут себя совершенно различным образом в области рас - р слоения на две фазы. Вместо S-образного завитка на изотерме Ван-дер - Ваальса реальная изотерма имеет в этой области прямолинейный горизонтальный участок, который располагается так, что охватываемые завитком площади Рг и F2 ( рис. 124.2) одинаковы. [19]
Таким образом, изотермы Ван-дер - Ваальса не только более точно, чем изотерма идеального газа, передают поведение газа, но охватывают собою и процесс ожижения газов, а также выражают то свойство жидкости, которое проявляется в ее малой сжимаемости. [20]
Поэтому-то кучасткуСВне подходит обычная изотерма ван-дер - Ваальса для неизменной массы вещества. [21]
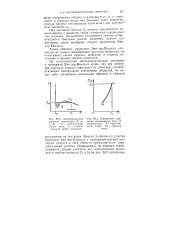
Вместо S-образпого участка изотермы Ван-дер - Ваальса у экспериментальной изотермы имеется в этой области прямолинейный горизонтальный участок. Основываясь на законах термодинамики, можно доказать, что охватываемые впадиной и горбом площади S и S2 на рис. 88.2 одинаковы. [23]
Общий характер изменения изотерм Ван-дер - Ваальса с температурой виден на рис. 88 ( по оси абсцисс отложен удельный объем), на котором представлен в качестве примера ряд изотерм для углекислоты. [24]
 |
Заштрихованные [ IMAGE ] Зависимость дав. [25] |
Вместо S-образного участка изотермы Ван-дер - Ваальса у экспериментальной изотермы имеется в этой области прямолинейный горизонтальный участок. Основываясь на законах термодинамики, можно доказать, что охватываемые впадиной и горбом площади Si и S2 на рис. 88.2 одинаковы. [26]
С помощью семейства изотерм Ван-дер - Ваальса на диаграмме p ( V) ( рис. 10) найти постоянные коэффициенты а и b в уравнении Ван-дер - Ваальса, если заданы критическая температура и критическое давление реального газа, подчиняющегося уравнению Ван-дер - Ваальса. [27]
Точки участка г-д изотермы Ван-дер - Ваальса соответствуют физически однородному состоянию вещества ( фазе), называемому перегретой жидкостью. Перегретая жидкость - это метастабилъное, обладающее ограниченной устойчивостью состояние. При специальных условиях такое состояние жидкости может быть реализовано на практике. Перегретая жидкость существует лишь до тех пор, пока эта ме-тастабильная фаза не граничит с другой, более устойчивой фазой. Так, перегретая жидкость закипает, если в нее попадают пузырьки какого-либо газа или пара самой жидкости. Явление вскипания перегретой жидкости используется для наблюдения следов ( треков) ионизирующих частиц с помощью так называемой пузырьковой камеры. [28]
Общий характер изменения изотерм Ван-дер - Ваальса с температурой виден на рис. 88 ( по оси абсцисс отложен удельный объем), на котором представлен в качестве примера ряд изотерм для углекислоты. [29]
Страницы: 1 2 3 4