Изотерма - адсорбция - пар - вода
Cтраница 4
Изотермы адсорбции паров воды на силикагеле обычно обладают ярко выраженной петлей гистерезиса; однако Пэтрик [68] нашел, что эта петля исчезает, если предварительно эвакуировать атот гель при 350, до прекращения выделения газов. [46]
Применение цеолитов КА для осушки легкополимеризующихся углеводородов ( диенов, ацетиленовых) перспективно, но требуется создать условия получения термостабильных сорбентов этого типа, а также уточнить оптимальный режим их регенерации. Поскольку изотермы адсорбции паров воды на калиевой форме цеолита А более пологи в облас и малых концентраций, чем на NaA, следует полагать, что и температура десорбции воды может быть соответственно понижена. [47]
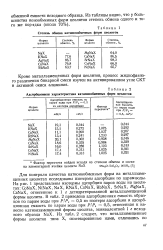 |
Степень обмена катионообмешых форм цеолитов.| Адсорбционная характеристика катионообменных форм цеолитов. [48] |
Для контроля качества катионообменных форм на металлзамещенных цеолитах исследованы изотермы адсорбции по парам воды. На рис. 1 представлены изотермы адсорбции паров воды на цеолитах: CoNaX, NiNaX, NaX, KNaX, CuNaX, RbNaX, SrNaX, MgNaX, CaNaX, отнесенные к 1 г дегидратированной металлзамещенной формы цеолита. В табл. 2 приведена адсорбционная емкость образцов по парам воды при PJPS 0 5 из изотерм адсорбции и адсорбционная емкость по парам воды при PJPS 0 5, отнесенная к навеске катионзамещенной формы цеолита, эквивалентной 1 г исходного образца NaX. [49]
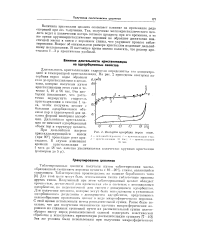 |
Изотермы адсорбции паров воды. [50] |
Длительность кристаллизации гидрогеля определяется его концентрацией и температурой кристаллизации. На рис. 2 приведены изотермы адсорбции паров воды образцом, геля до кристаллизации и цеолн - тами, которые получены путем кристаллизации этого геля в течение 1, 10 л 96 час. Эти изотермы показывают, что достаточно подвергнуть гидрогель кристаллизации в течение 1 часа, чтобы получить цеолит с большим адсорбционным объемом пор и характерной для це - н олита формой изотермы адсорбции. Дальнейшая кристаллизация не изменяет адсорбционный объем пор и структуру цеолита. [51]
Термическая устойчивость образцов изучена в области температур 300 - 800 С. На дегидратированных цеолитах исследованы изотермы адсорбции паров воды при 20 С. После нагревания в воздухе при соответствующей температуре в течение 4 часов образцы перед снятием изотерм сорбции прогревались в вакуумной установке при температуре 300 в течение 4 часов. При температуре 600 С проведены дополнительные опыты по определению термической устойчивости различных ионообменных форм цеолитов в зависимости от продолжительности прокаливания. [52]
 |
Классификация изотерм адсорбции по Брунауэру. [53] |
Во многих случаях возникают трудности при определении угла смачивания ф, который для различных паров зависит от вида и количества кислородных соединений на поверхности угля. Влияние угла Ф на изотерму адсорбции паров воды показано на рис. 3.5, при этом изотерма измерялась на свежепрокаленном, необработанном и покрытом поверхностными оксидами активном угле. [54]
Из этой кривой видно, что этот образец очень слабо адсорбирует воду: величины адсорбции весьма малы и изотерма оказывается даже вогнутой. Эта изотерма сходна с изотермой адсорбции пара воды на силикагеле, прокаленном при температуре 650 С. [55]
 |
Изотермы адсорбции паров воды на гранулированном цеолите NaA. [56] |
Адсорбция воды на цеолитах имеет ряд характерных особенностей. На рис. 1 - 31 представлены изотермы адсорбции паров воды на цеолите NaA. Для всех цеолитов характерен очень крутой подъем изотерм в области малых концентраций паров воды. Адсорбционная способность цеолитов при обычных температурах уже при давлении 130 - 260 Па ( 1 - 2 мм рт. ст.) близка к адсорбционной способности при максимальном насыщении. Даже в области очень малых давлений влага адсорбируется в значительных количествах. Так, при температуре 25 С и давлении 13 30; 1 33; 0 13 Па ( 10 -, lO 2, 10 - 3 мм рт. ст.) адсорбционная емкость по парам воды составляет соответственно 15, 6 и 3 г на 100 г цеолита NaA. Эта особенность указывает на перспективность использования цеолитов для осушки газов, содержащих водяные пары в небольшом количестве. [57]
Исследования сорбционных свойств полученных цеолитов производили на вакуумных весовой и объемной сорбциоиных установках. Эти исследования позволяли получить данные об общем объеме пор пористых кристаллов из изотерм адсорбции паров воды и охарактеризовать типичные синтезированные образцы в отношении их способности к селективной адсорбции. [58]
Подобная идеализированная ситуация, конечно, фактически не имеет места в реальных силикагелях, поры в которых представляют собой неправильной формы пространства между беспорядочно расположенными первичными сферическими частицами кремнезема. В качестве примеров, связанных с применением на практике таких систем, на рис. 5.10 показаны изотермы адсорбции пара воды и соответствующие кривые распределения пор по размерам, рассматриваемые Киселевым [146] для серии силикагелей, каждый из которых имеет относительно однородные по размерам поры. Объемы пор оказались по существу одинаковыми для силикагелей 2 и 3 и для силикагелей 4 и 5, что подтверждается примерно одинаковым количеством воды, требуемой для заполнения пор. Площади под кривыми распределения пор по размерам для тех же двух образцов 2 и 3 примерно равны и также выражают значение, равное 0 9 см3 / г. Эти изотермы характерны для типов силикагелей, приготовляемых стандартными способами. [59]
 |
Изотермы адсорбции паров воды при температуре 209 С на различных ионообменных формах цеолита типа X. [60] |
Страницы: 1 2 3 4 5