Установление - равновесный потенциал
Cтраница 3
Для определения малых количеств фторидов в различных объектах чаще всего применяют методы прямой потенциометрии, используя такие достоинства фтор-селективного электрода, как высокая селективность, достаточно низкий предел обнаружения, малая продолжительность установления равновесного потенциала, стабильность градуировочного графика. [31]
К анализируемому раствору добавляют 1 г бифталата калия, 0 5 г фторида натрия, разбавляют водой до 100 мл и титруют раствором дитиоксамида с 2 - 3-минутными промежутками между добавлением порции титранта для установления равновесного потенциала. После каждого титрования серебряный электрод механически очищают от окисной пленки погружением в 0 05 М раствор роданида калия на 1 мин. [32]
Рядом исследователей [14, 15] проведены работы по экспериментальному изучению динамических характеристик стеклянных электродов. Инерционность установления равновесного потенциала в электродной системе определяется в основном тремя факторами: наличием емкости между электродами и в соединительном кабеле, скоростью миграции свободных Н между средой и стеклянной мембраной и характером диффузии Н и ОН в приэлектродном ламинарном слое жидкости. Последний фактор в значительной степени определяется условиями перемешивания измеряемой среды. [33]
Рядом исследователей [14, 15] проведены работы по экспериментальному изучению динамических характеристик стеклянных электродов. Инерционность установления равновесного потенциала в электродной системе определяется в основном тремя факторами: наличием емкости между электродами и в соединительном кабеле, скоростью миграции свободных Н между средой и стеклянной мембраной и характером диффузии Н и ОН - в приэлектродном ламинарном слое жидкости. Последний фактор в значительной степени определяется условиями перемешивания измеряемой среды. [34]
 |
Кривые потенциометрического титро - р. [35] |
Время установления равновесного потенциала индикаторных электродов мало, что удобно для изучения кинетики реакций и автоматического контроля технологических процессов. [36]
Сначала ти-трант приливают из бюретки по каплям быстро, а по мере приближения к точке эквивалентности - по 0 05 мл, допускается приливание по 0 04 мл или 0 06 мл. Каждый раз после установления равновесного потенциала записывают показания потенциометра в милливольтах против прилитого объема. Скачок устанавливают по наибольшему изменению потенциала от введения вышеуказанного объема титранта. При двух одинаковых наибольших значениях изменения за скачок принимают первое значение. [37]
Установление равновесного потенциала связано с обменом между металлом и его ионами в растворе. Таким образом, для установления равновесного потенциала на металлическом электроде необходимо присутствие его ионов в растворе и отсутствие побочных обменных реакций. Время установления потенциала зависит от скорости обмена. [38]
В данном случае процесс установления равновесного потенциала определяется не свойствами мембраны, а абсорбцией более концентрированного раствора на поверхности измерительного сосуда, мембраны, электролитического ключа. [39]
Показано, что мембранные электроды на основе этой системы ( аликвот 336 S деканол) обратимы относительно анионов ClOi, SCN, I, NOa, Br -, СГ, Ac, SOl и фосфатных ионов, а также некоторых органических. Отмечена хорошая воспроизводимость и быстрота установления равновесного потенциала. Однако в качестве ионоселективных эти электроды пригодны только для следующих анионов: ClOi, SCN, Г, МОз, Вг -, С1, а для анионов Ac, SOl и фосфатных можно отметить только способность мембраны реагировать на изменение концентрации последних в чистых растворах соответствующих солей. [40]
Существенным недостатком этого метода является необходимость работы в атмосфере инертного газа и связанная с этим громоздкость аппаратуры. Кроме того, требуется время для установления равновесного потенциала после добавления каждой порции окислителя. [41]
Накопление заряда на мишени происходит в течение некоторого времени. Длительность этого процесса, приводящего к установлению равновесного потенциала мишени, зависит от разности между начальным и равновесным потенциалом, величины емкости заряжаемого элемента мишени относительно других электродов, величины тока луча. Чем больше ток луча, тем быстрее происходит накопление заряда. Если луч воздействует на мишень кратковременно, то возможно только некоторое смещение потенциала элемента мишени в сторону равновесного. Поэтому если луч не неподвижен, а развертывается по мишени, то по всей трассе его движения происходит смещение потенциала, который может достигать равновесного только при достаточно большой плотности тока первичных электронов, зависящей от величины тока луча, размеров электронного пятна на мишени и скорости его перемещения. Чем больше ток луча, лучше его фокусировка и меньше скорость, тем ближе к равновесному смещаются потенциалы участков мишени, лежащих по трассе луча. [42]
Как показала эта серия опытов, время установления равновесного потенциала ( рН) существенно зависит от скорости перемешивания раствора, величины газового зазора, концентрации кислоты и составляет при максимально большой скорости перемешивания и минимальном зазоре ( оптимальные условия) для больших концентраций кислоты - 30 мин, для минимальных концентраций кислоты - 10 мин. [43]
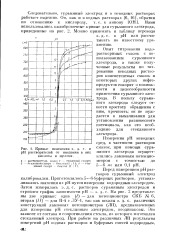 |
Кривые изменения э. д. с. и. [44] |
В пользу сурьмяного электрода следует отнести простоту обращения с ним, прочность: он не нуждается в вымачивании для установления равновесного потенциала, как это необходимо для стеклянного электрода. [45]
Страницы: 1 2 3 4