Устойчивость - золи
Cтраница 1
Устойчивость золей в основном зависит от заряда коллоидных частиц. [1]
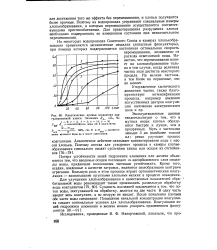 |
Кинетические кривые осаждения коагулированной взвеси. Значения Ддч / Дк, %. [2] |
Потеря устойчивости золей гидроокиси алюминия или железа объясняется тем, что вводимые осадки поглощают из адсорбционного слоя мицеллы ионы, придающие коллоидным частицам устойчивость. Кроме того, осадки, введенные в качестве затравок, являются своеобразными центрами агрегации. Большую роль в этом процессе играет ортокинетическая коагуляция - захватывание крупными хлопьями мелких в процессе осаждения. Сущносгь последней заключается в том, что поток воды, поступающей на обработку, делится на две части В одну часть, вводят весь коагулянт, а во вторую не вводят. После появления хлопьев обе части воды смешивают. Повышение начальной концентрации коагулянта создает оптимальные условия для хлопьеобразования. [3]
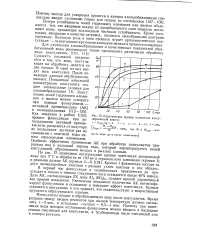 |
Кинетические кривые осаждения коагулированной взвеси. [4] |
Потеря устойчивости золей гидроокиси алюминия или железа объясняется тем, что вводимые осадки из адсорбционного слоя мицеллы поглощают ионы, придающие коллоидным частицам устойчивость. Кроме того, осадки, введенные в качестве затравок, являются своеобразными центрами агрегации. Большую роль в этом процессе играет ортокинетическая коагуляция - захватывание крупными хлопьями мелких в процессе осаждения. [5]
Однако обычно устойчивость золей связывают не со значением о а с величиной штерновского потенциала 4 5, равного потенциалу одиночного двойного слоя Ф, который часто отождествляют с f - потенциалом. [6]
 |
Влияние концентрации дисперсной фазы на устойчивость золей Agl, содержащих добавки КМЦ-300. [7] |
Поскольку изменение устойчивости золей в присутствии КМЦ непосредственно связано с адсорбцией молекул ( ионов) полиэлектролита дисперсной фазой, то важно установить, какая доля введенных в золь макромолекул адсорбируется коллоидными частицами и какое покрытие их поверхности молекулами КМЦ обеспечивает стабилизацию коллоидного раствора. Это может быть осуществлено косвенным путем - на основании данных о влиянии концентрации дисперсной фазы на устойчивость золя [12] в присутствии полиэлектролита. Поскольку при разбавлении золя степень дисперсности остается, по-видимому, неизменной, то уменьшение концентрации дисперсной фазы эквивалентно такому же уменьшению суммарной адсорбирующей поверхности. Отсюда, зная удельную поверхность дисперсной фазы, можно определить площадь, приходящуюся на одну адсорбированную молекулу КМЦ, и сделать некоторые предположения относительно ориентации макромолекул на поверхности частиц. [8]
Разобрав вопрос об устойчивости золей к агрегации, мы не можем не остановиться на вопросе о связи ее с устойчивостью кинетической. Эти два вида устойчивости по своему существу противоположны, однако это различие ни в какой степени не дает основания рассматривать их независимо друг от друга. Говорить о кинетической устойчивости отдельно и независимо от агрегативной не вполне правильно, и, прежде всего, потому, что между этими противоположными видами устойчивости существует вполне определенная и ясная связь. [9]
Разобрав вопрос об устойчивости золей к агрегации, мы не можем не остановиться на вопросе о связи ее с устойчивостью кинетической. [10]
Совершенно иной характер устойчивости золей при гидрофильной поверхности коллоидных частиц, которая обусловливает образование молекулярных сольватных слоев при участии вандерваальсовых, водородных и комплексных связей, вне зависимости от действия небольших концентраций электролитов. [11]
Совсем другой характер имеет устойчивость золей, если поверхность коллоидных частиц сама является гидрофильной или способна к образованию молекулярных сольват-ных слоев при участии Ван-дер - Ваальсовых, водородных и комплексных связей, сравнительно устойчивых к действию электролитов небольших концентраций. В этом случае даже при переходе порога коагуляции коллоидные частицы могут сохраниться в состоянии золя, если они обладают достаточной гидрофильностью. [12]
Совсем другой характер имеет устойчивость золей, если поверхность коллоидных частиц сама является гидрофильной или способна к образованию молекулярных сольватных слоев при участии ван-дер-ваальсовых, водородных и комплексных связей, сравнительно устойчивых к действию электролитов небольших концентраций. В этом случае даже при переходе порога коагуляции коллоидные частицы могут сохраниться в состоянии золя, если они обладают достаточной гидрофильностью. [13]
Вещества, вызывающие повышение устойчивости суспензоид-ных золей, называются защитными коллоидами. [14]
В трактовке причин изменения устойчивости золей ППК с изменением рН мнения авторов также резко расходятся. Айлер [2] не учитывает связи ИЭТ с устойчивостью и считает причиной максимума стабильности золей ПКК следовые примеси фторид-иона и катионов - комплексообразовате-лей в золях. Ряд авторов [5, 6] полагает, что наиболее устойчивыми золи ПКК должны быть в ИЭТ, так как, по их мнению, появление ионов силиката с ростом рН ускоряет каталитический процесс полимеризации ПКК; эти исследователи оставляют вне поля зрения взаимодействие ПКК с дисперсионной средой - водой. [15]
Страницы: 1 2 3 4