Устойчивость - золи
Cтраница 4
Очевидно, что лишение коллоидных частиц их электрического заряда ( хотя бы частичное) должно понижать устойчивость золей и способствовать их коагуляции. Такое разряжение в случае гидрозолей может быть проще всего достигнуто добавлением к коллоидному раствору электролитов. Хотя при этом вводится одинаковое число положительных и отрицательных зарядов, по в непосредственно окружающей коллоидную частицу ионной атмосфере всегда несколько преобладают ионы, противоположно заряженные, которые частицей преимущественно и адсорбируются. Так как введение электролита сильно повышает общую концентрацию ионов в растворе, условия для их адсорбции становятся весьма благоприятными и первоначальный заряд частиц быстро нейтрализуется, следствием чего является коагуляция золя. Природный процесс коагуляции электролитами широко осуществляется в устьях рек, где приносимые ими коллоиды и взвеси осаждаются под действием солей морской воды. [46]
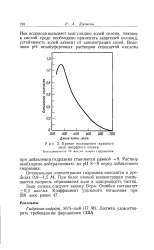 |
Кривая поглощения красного золя аморфного селена. [47] |
Ион водорода вызывает коагуляцию золей селена, поэтому в кислой среде необходимо применять защитный коллоид; устойчивость золей зависит от концентрации солей. [48]
Очевидно, что снятие с коллоидных частиц их электрического заряда ( хотя бы частичное) должно понижать устойчивость золей и способствовать их коагуляции. Такое разряжение в случае гидрозолей может быть проще всего достигнуто добавлением к коллоидному раствору электролитов. Хотя при этом вводится одинаковое число положительных и отрицательных зарядов, в непосредственно окружающей коллоидную частицу ионной атмосфере всегда несколько преобладают ионы, противоположно ей заряженные, которые частицей преимущественно и адсорбируются. Так как введение электролита сильно повышает общую концентрацию ионов в растворе, условия для их адсорбции становятся весьма благоприятными и первоначальный заряд частиц быстро нейтрализуется, следствием чего является коагуляция золя. Природный процесс коагуляции электролитами широко осуществляется в устьях рек, где приносимые последними коллоиды и взвеси осаждаются под действием солей морской воды. [49]
Изучая коацервацию ( расслаивание) золей, Кроит вынужден признать, что и при наличии, гидратации устойчивость золей нарушается и что если при коацервации и имеет место дегидратация, то она связана только с отрывом поверхностных слоев растворителя от частицы и приводит к превращению диффузной оболочки в резко ограниченную оболочку, отличающуюся от первой только своей наружной частью. Очень близкие, хотя и не вполне тождественные воззрения защищает Песков. Коагуляцию лиофильных коллоидов этот исследователь разбивает на два типа, резко отличающиеся друг от друга. [50]
Очевидно, что снятие с коллоидных частиц их электрического заряда ( хотя бы частичное) должно понижать устойчивость золей и способствовать их коагуляции. [51]
Таким образом, на основании исследования коллоидных и сорб-ционных свойств гидратнрованных окисей титана авторы предположили, что устойчивость золей в концентрированных распюрах соляной кислоты обусловлена сольватацией частиц дисперсной фазы. [52]
Страницы: 1 2 3 4