Устойчивость - золи
Cтраница 2
Особый интерес представляет механизм устойчивости золей двуокиси титана. Устойчивость полученных нами золей не может быть объяснена отталкиванием ионных сфер, поскольку при концентрации электролита ( соляной кислоты) порядка 1 моль. [16]
Изменение температуры различно влияет на устойчивость золей. В то время как одни из них ( например, As Sa) при нагревании легко коагулируют, другие ( например, РегОз) не изменяются даже при длительном кипячении. В общем можно сказать, что для большинства неорганических коллоидов нагревание заметно способствует коагуляции. Одной из важнейших причин этого является уменьшение при нагревании адсорбции ионов коллоидными частицами, что влечет за собой понижение их заряда. [17]
Изменение температуры различно влияет на устойчивость золей. В то время как одни из них ( например, As2S3) при нагревании легко коагулируют, другие ( например, Fe2O3) не изменяются даже при длительном кипячении. В общем можно сказать, что для большинства неорганических коллоидов нагревание заметно способствует коагуляции. Одной из важнейших причин этого является уменьшение при нагревании адсорбции ионов коллоидными частицами, что влечет за собой понижение их заряда. [18]
Из сравнения приведенных данных по устойчивости золей и сопоставления литературных данных по сорбнруемостп ионов хлора, сульфата и фосфата на двуокиси титана [3. 7-9, 11, 12] видно, что между стабильностью золей и сорбируемостыо анионов существует симбатная зависимость. Аналогичная зависимость имеет место и для катионов. [19]
Серия работ А. В. Думанского посвящена изучению устойчивости золей в присутствии электролитов. [20]
По современным представлениям основная причина устойчивости золей обусловлена наличием сольватных ( гидратных) оболочек у ионов диффузного слоя. Обладая упругими свойствами, эти оболочки препятствуют слипанию частиц. [21]
 |
Схема строения мицеллы иодида серебра. / - ядро ( А. 2 - адсорбционный слой. 3 - ( а - К - адсорбционный слой. 4 - диффузионный слой. [22] |
У типичных лиофобных коллоидных систем агрегатив-ная устойчивость золей зависит от тех ионов, которые адсорбированы на поверхности их частиц. [23]
Добавка высокомолекулярных веществ не всегда повышает устойчивость золей. У некоторых коллоидных растворов они понижают пороги коагуляции и даже вызывают коагуляцию. Повышенная чувствительность коллоидного раствора к коагулирующим электролитам носит название сенсибилизации. [24]
Исследование влияния природы аниона кислоты-осадителя на устойчивость золей показало ( см. таблицу), что положение максимума устойчивости закономерно изменяется при изменении основных физико-химических характеристик кислоты. Такое смещение положения ИЭТ золей ПКК с изменением среды может быть следствием изменения электронодонорных свойств аниона, хотя не исключена возможность того, что определенное значение имеет также необходимое для достижения одного и того же рН увеличение концентрации кислоты-осадителя по мере уменьшения степени ее ионизации. [25]
При исследовании влияния поверхностно-активных веществ на устойчивость золей AgBr, было найдено, что метиловый эфир полиэтиленгликоля незначительно повышает устойчивость коллоидных растворов бромида серебра. Это означает, что в присутствии плохо адсорбируемого частицами метилового эфира полиэтилен-гликоля золи AgBr остаются ионно стабилизованными. [26]
При исследовании влияния поверхностно-активных веществ на устойчивость золей AgBr, было найдено, что метиловый эфир полиэтиленгликоля незначительно повышает устойчивость коллоидных растворов бромида серебра. Даже при относительно высоком содержании эфира значения порога коагуляции золей ионами разной валентности резко отличались между собой. Это означает, что в присутствии плохо адсорбируемого частицами метилового эфира полиэтилен-гликоля золи AgBr остаются ионно стабилизованными. [27]
Дзета-потенциал является одним из важнейших факторов устойчивости золей. Всякие изменения величины и знака электрокинетического потенциала могут привести к существенным изменениям в золях, вплоть до разрушения коллоидного раствора с выпадением дисперсной фазы в осадок ( процесс коагуляции. [28]
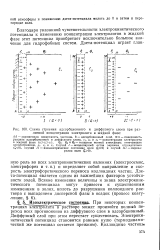 |
Схема строения адсорбционного и диффузного слоев при различной концентрации электролита в жидкой фазе. [29] |
Дзета-потенциал является одним из важнейших факторов устойчивости золей. [30]
Страницы: 1 2 3 4