Устойчивость - комплекс - металл
Cтраница 1
Устойчивость комплексов металлов с EDTA обычно уменьшается с увеличением ионных радиусов ( негидратированных ионов), и соответственно этому возрастает степень вытеснения со смолы ионов меньшего размера, правда, с некоторыми исключениями. [1]
Устойчивость комплексов металла с аминогруппой в катионо-обменнике зависит от ряда факторов. Амины с большой молекулой не проникают в смолу; молекулы ароматических аминов, особенно бензиламин, сорбируются смолой типа полистирольной, и в результате этого внутри смолы их комплексы с металлами становятся устойчивее. Очень интересен случай с 1 2-диаминами. Судя по кривой зависимости п в смоле от логарифма концентрации диамина в растворе, комплекс серебра ( 1) с этилендиамином в 103 раз прочнее в смоле, чем в растворе; однако каждый ион серебра в смоле координирован только с одной молекулой этилендиамина [30], тогда как в растворе он соединен с двумя молекулами. Возможно, что в смоле этилендиамин реагирует как мостиковый лиганд с образованием длинного полиядерного комплекса. Полиядерные комплексы, вероятно, образуются и при ассоциации никеля ( П) с гидразином. Здесь упрочнение не превышает 1 5 логарифмической единицы, но максимум насыщения достигается при четырех молекулах гидразина на ион никеля вместо шести, как это имеет место в разбавленных водных растворах. Это дает повод считать, что два гидразина шестикоординационного никеля в двумерной структуре исполняют роль мостиковых лигандов. Интересным представляется тот факт, что степень набухания и содержание воды в сульфокислотных смолах, насыщенных никелем и гидразином, значительно меньше нормальных. [2]
Устойчивость комплексов металлов с ЭДТА зависит от рН раствора. При рН 9 25 оба металла образуют прочные комплексы. На этом основано их совместное определение. [3]
Устойчивость комплексов металлов с некоторыми С-замещенными производными глицина. [4]
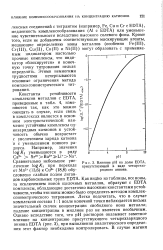 |
Влияние рН на долю EDTA, присутствующей в виде четырехзарядного аниона. [5] |
Константы устойчивости комплексов металлов с EDTA, приведенные в табл. 4, изме-няются так, как это можно ожидать в случае, если связь в комплексах является в основ-ном электростатической: наименее устойчивы комплексы однозарядных катионов и устойчивость обычно возрастает с увеличением заряда катиона и с уменьшением ионного радиуса. Сравнительно небольшое увеличение log / Ci при переходе от Мп2 ( 13 6) к Си2 ( 18 8) обусловлено слабым полем лиган-дов карбоксильных групп EDTA. Как видно из таблицы, все ионыг за исключением ионов щелочных металлов, образуют с EDTA комплексы, обладающие достаточно высокими константами устойчивости, чтобы эти ионы можно было определять методом комплексонометрического титрования. Легко подсчитать, что в случае комплексов состава 1: 1 возле конечной точки наблюдается весьма значительный скачок концентрации свободного иона металла; падение концентрации в миллион раз не является необычным. Однако вследствие того, что рН растворов оказывает заметное влияние на концентрацию присутствующего четырехзарядного аниона EDTA ( рис. 3), при выполнении аналитического определения этот фактор необходимо контролировать. [6]
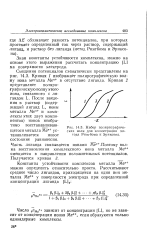 |
Набор полярографических волн для иллюстрации метода Рингбома и Эриксона. [7] |
Константы устойчивости комплексов металла Меп можно определить относительно просто. [8]
 |
Измерение конусного угла лиганда в соединении LA. [9] |
Сопоставление устойчивости изоструктурных комплексов металлов, стоящих друг над другом в периодической системе, позволяет заметить одну интересную закономерность. [10]
Например, устойчивость комплексов металлов группы а изменяется для атомов элементов VA - VIIА групп следующим образом: N Р As Sb, О S Se Те, F Cl Br I. Устойчивость комплексов металлов группы б изменяется в обратной последовательности. [11]
Поэтому константы устойчивости комплексов металлов представляют большой теоретический и практический интерес. Недавно Бьерру-мом, Шварценбахом и Силленом были изданы [3] таблицы всех: констант устойчивости, имеющихся в литературе. [12]
Эффективная константа устойчивости комплекса металла с титрантом должна быть значительно больше аналогичной константы комплекса с индикатором - т - по меньшей мере на сорок процентов. [13]
Впервые константы устойчивости комплексов металлов были опубликованы в начале XX столетия. [14]
В общем случае эффективная устойчивость комплекса металла с индикатором должна быть меньше, чем эффективная устойчивость комплекса данного металла с титрантом. [15]
Страницы: 1 2 3 4