Устойчивость - комплекс - металл
Cтраница 3
Значение обоих факторов - кислотности и жесткости-мягкости - показано на рис. 8.3 на примере изменения устойчивости комплексов металлов ряда Ирвинга - Уильямса с некоторыми лигандами. Ряд Ирвинга - Уильямса для возрастающей устойчивости комплексов Ва2 - Си2 отражает увеличение присущей металлам кислотности главным образом из-за уменьшения размеров ионов. При переходе к более мягкому иону Zn2 наблюдается снижение устойчивости. [31]
Это значит, что влияние комплексообразования на окислительно-восстановительные потенциалы ионов металлов непосредственно связано с различиями констант устойчивости комплексов металлов в рассматриваемых валентных состояниях. Иногда наблюдаются весьма значительные эффекты. Это же справедливо и для комплексов Си ( II), что указывает на возможное применение таких комплексов в качестве восстановителей в титриметрическом анализе. [32]
Наиболее существенным доказательством схемы (4.39) - 4.4 1) и уравнения (4.42) является найденная на этой основе константа устойчивости комплекса металла с высшей степенью окисления с субстратом-окислителем, которая оказалась близкой к соответствующей константе устойчивости, полученной другими ( неэлектрохимическими) методами. [33]
Если логарифмы константы устойчивости комплекса металла с индикатором, отрицательный логарифм начальной концентрации титруемого металла и логарифм константы устойчивости комплекса металла с комплексоном III отличаются примерно-на единицу, то ошибка титрования будет незначительной. Если же указанные параметры отличаются друг от друга в меньшей степени, то ошибка титрования может значительно возрасти. Этим условием определяется наименьшая; концентрация титруемого металла. [34]
Если логарифмы константы устойчивости комплекса металла с индикатором, отрицательный логарифм начальной концентрации титруемого металла и логарифм константы устойчивости комплекса металла с комплексоном III отличаются примерно на единицу, то ошибка титрования будет незначительной. Если же указанные параметры отличаются друг от друга в меньшей степени, то ошибка титрования может значительно возрасти. Этим условием определяется наименьшая концентрация титруемого металла. [35]
Из этих выражений следует, что количество сорбированных ионов металла зависит от общего количества ионов в водной фазе, устойчивости комплекса металла и концентрации избытка лиганда. [36]
Образуется лишь небольшое количество комплекса металла, и скорость реакции зависит от его концентрации или, другими словами, от устойчивости комплекса металла. [37]
 |
Классификация катионов в зависимости от числа электронов во внешней оболочке ( п и ионного потенциала ( z / r, где г измеряется в А. [38] |
Катионы группы В с более низкими ионными потенциалами и оболочками из 18 электронов, легко поляризующиеся и образующие комплексы, устойчивость которых часто превышает устойчивость комплексов металлов группы А. [39]
Когда число слагаемых, стоящих под знаком тройных сумм в уравнениях (11.106) - (11.108), невелико, причем слагаемые, учитывающие не связанные в комплексы лиганды, известны из ацидо-метрических определений, то исходя из указанных уравнений, можно выразить в простых случаях концентрацию [ Мг ] через общие концентрации ионов металла и лиганда, концентрацию ионов водорода и неизвестные константы устойчивости комплексов металла. [40]
В образующемся красном комплексе - хелате - имеется координационная связь иона металла с атомом азота азогруппы и валентная с двумя оксигруппами в о-положении к ней. Устойчивость комплексов металлов с металлоинди-катором должна быть меньше устойчивости соответствующих комплексонатов. На рис. 15.8 в качестве примера приведены электронные спектры поглощения эриохромового черного Т и его комплекса с магнием. Из них следует, что свободный индикатор наиболее интенсивно поглощает лучи красного цвета и имеет, следовательно, синюю окраску. Комплекс магния с реагентом более погло: щает желто-зеленое излучение и поэтому отличается красно-фиолетовой окраской. [41]
Например, устойчивость комплексов металлов группы а изменяется для атомов элементов VA - VIIА групп следующим образом: N Р As Sb, О S Se Те, F Cl Br I. Устойчивость комплексов металлов группы б изменяется в обратной последовательности. [42]
Чем больше различаются устойчивости комплексов разделяемых металлов, тем более эффективно применение Н - формы смолы. [43]
Особенно часто обсуждаются зависимости констант устойчивости комплексов металлов от констант диссоциации или констант протоиирования органических реагентов. В пределах одного класса реагентов, кислотно-основные свойства которых изменяются за счет введения электроноактивиых заместителей в молекулу, наблюдается линейная зависимость между логарифмическими значениями констант устойчивости и константами Гаммета заместителей, характеризующими их электроиоактивиые свойства. [44]
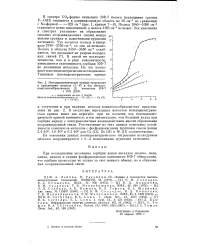 |
Потенциометрические кривые титрования. [45] |
Страницы: 1 2 3 4