Адсорбция - аргон
Cтраница 1
Адсорбция аргона мало чувствительна к химической природе поверхности. Из газов, обычно применяемых для определения поверхности ( азот, аргон, криптон, ксенон), аргон имеет наименьшую молекулу. Критическая температура двумерной конденсации для него ниже температуры жидкого азота, и поэтому осложнения, связанные с фазовыми переходами в адсорбционном слое, исключены. Хотя энергия адсорбционного взаимодействия для него ниже, чем, например, для азота, они достаточно велики, чтобы можно было пренебречь взаимодействием адсорбат - адсорбат вдоль поверхности и применять уравнение метода БЭТ для расчета величины поверхности. [1]
Изотермы адсорбции аргона на сульфате меди и сульфате алюминия, начерченные согласно потенциальной теория. [2]
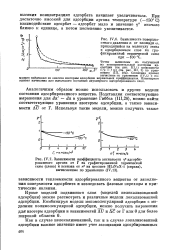
Теплоты адсорбции аргона кислорода и азота, на рутиле заметно падают с увеличением количества адсорбированного вещества [179], На рис. 25 изображены полученные на основе данных Моррисона и его сотрудников [180] кривые, выражающие зависимости изостер-ных теплот адсорбции азота ( кривая 5) и аргона ( кривая 4) от степени заполнения, приведенные к 0 К. Эти кривые аналогичны по своему характеру, что позволило Дрэйну и Моррисону [376] путем линейного преобразования привести их к одной кривой. Соответ - Д ствующую кривую для кисло - § рода также можно было бы s привести к той же кривой. [3]
Вычисление рм для адсорбции аргона на меди на основании уравнения ( 75) дает величину в 27 50 кал) моль, если мы снова примем г 3 2 А. Эта величина очень близка к экспериментальной теплоте адсорбции. [4]
Вычисление pDS для адсорбции аргона на меди на основании уравнения ( 75) дает величину в 2750 кал / моль, если мы снова примем г 3 2 А. Эта величина очень близка к экспериментальной теплоте адсорбции. [5]
Юрри [53] измерял адсорбцию аргона, кислорода и метана на силикагеле при температурах, лежащих в интервале от 90 до 273 К. Он нашел, что изотермы подчиняются уравнению Фрейндлиха. [6]
Примером тому может служить адсорбция аргона на шабазите. Как и при адсорбции С02, изостерическая теплота, вначале высокая, быстро падает по мере заполнения объема полостей, проходит через минимум, после чего вновь достигает максимума. [7]
При достаточно высокой для адсорбции аргона температуре ( - 150 С) взаимодействие адсорбат - адсорбат мало и значение у8 вначале близко к единице, а потом постепенно увеличивается. [9]
Таким образом, время адсорбции аргона на угле, несмотря на несколько более высокую теплоту адсорбции и более низкую температуру опыта, практически совпадает со временем адсорбции ксенона на ртути. Следовательно, если все прочие параметры, такие, как температура и теплота адсорбции, сохраняются неизменными, то чем выше энтропия, тем подвижнее адсорбированная молекула и тем больше время ее адсорбции. [10]
Таким образом, время адсорбции аргона на угле, несмотря на несколько более высокую теплоту адсорбции и более низкую температуру опыта, практически совпадает со временем адсорбции ксенона на ртути. [11]
Рассмотрим в качестве примера адсорбцию аргона на базисной грани графита. [12]
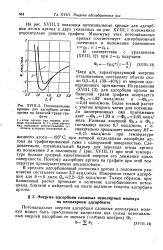 |
Потенциальные кривые для адсорбции атома аргона на базисной грани графита. [13] |
С, при которой исследована адсорбция аргона на графитированной саже с однородной поверхностью. [14]
На рис. 4 приведены изотермы адсорбции аргона и паров бензола и - гептана. Бензол, как и следовало ожидать, не адсорбируется цеолитом 5А вследствие того, что размеры его плоской молекулы оказались крупнее, чем входы в большие полости. [15]
Страницы: 1 2 3 4