Адсорбция - аргон
Cтраница 4
В наших опытах интервал температур, при которых происходит адсорбция кислорода, всегда был шире, чем при адсорбции аргона. [46]
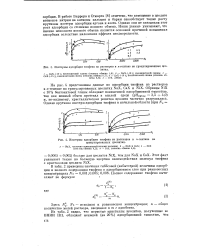 |
Изотермы адсорбции тиофена из растворов в w - гептане на гранулированных цеолитах.| Изотермы адсорбции тиофена из растворов в к-гептане на гранулированных цеолитах. [47] |
В работе Баррера и Стюарта [8] отмечено, что замещение в цеолите катионов натрия на катионы кальция и бария способствует также росту крутизны изотерм адсорбции аргона и азота. [48]
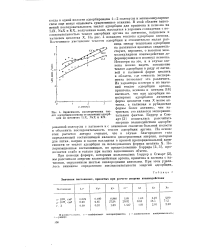 |
Зависимость изостерических теплот адсорбции ксенона от величины адсорбции на цеолитах LiX, NaX и КХ. [49] |
В этой области заполнений последовательность теплот адсорбции для криптона и ксенона на LiX, NaX и КХ, полученная нами, находится в хорошем совпадении с последовательностью теплот адсорбции аргона на литиевом, натриевом и калиевом цеолитах X. На рис. 4 показаны теплоты адсорбции ксенона. Постепенное увеличение теплоты адсорбции и относительно малая разница между теплотами адсорбции на различных цеолитах свидетельствуют, вероятно, о высоком межмолекулярном взаимодействии деформирующихся молекул ксенона. Несмотря на это, и в случае ксенона можно видеть повышение теплот адсорбции в ряду от литиевой к калиевой форме цеолита в области, где точность эксперимента позволяет это различить. Из характера изотерм и из значений теплот адсорбции аргона, криптона, ксенона и пентана [18] вытекает, что при адсорбции неполярных адсорбатов литиевая форма цеолитов типа X менее активна, а калиевая и рубидиевая формы более активны, чем натриевая; это является экспериментальным фактом. [50]
Понижение температуры приводит к уменьшению эффективного размера пор. Например, адсорбция аргона на цеолите 4А увеличивается с понижением температуры до - 150 С, а при дальнейшем понижении температуры - существенно уменьшается. Адсорбция полярных веществ также уменьшает эффективный размер пор. Например, предварительное насыщение цеолита 4А 5 % воды уменьшает его адсорбционную емкость к этилену в 35 раз. [51]
В большинстве случаев величина этого вклада мала. Например, для адсорбции аргона на хлориде калия он составляет только - 4 % вклада сил дисперсии. [52]
Хотя методы вычисления энергии взаимодействия между данной молекулой и ионным адсорбентом, с одной стороны, и той же молекулы и металлическим проводником - с другой, совершенно различны, эти различные трактовки приводят приблизительно к одним и тем же величинам теплоты. Так, для теплоты адсорбции аргона на йодистом калии вычисление дает 2100 кал / моль, для аргона на меди 2700 и для азота на угле 2400 кал / моль ( гл. Все эти значения являются, конечно, грубыми приближениями и несколько преуменьшенными по сравнению с экспериментальными теплотами адсорбции. [53]
Страницы: 1 2 3 4