Ван-дер-ваальсовая адсорбция
Cтраница 3
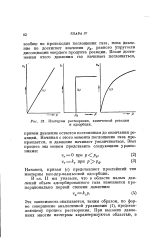 |
Изотермы растворения, химической реакции и адсорбции. [31] |
Наконец, кривая ( с) представляет простейший тип изотермы ван-дер-ваальсовой адсорбции. [32]
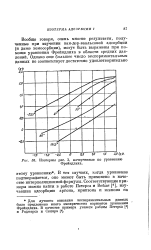 |
Изотермы 3, начерченные по уравнению Фрейндлиха. [33] |
Вообще говоря, очень многие результаты, полученные при изучении ван-дер-ваальсовой адсорбции ( и даже хемосорбции), могут быть выражены при помощи уравнения Фрейндлиха в области средних давлений. [34]
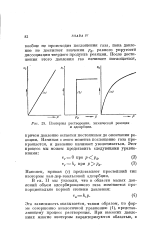 |
Изотермы растворения, химической реакции и адсорбции. [35] |
Наконец, кривая ( с) представляет простейший тип изотермы ван-дер-ваальсовой адсорбции. [36]
Вообще говоря, очень многие результаты, полученные при изучении ван-дер-ваальсовой адсорбции ( и даже хемосорбции), могут быть выражены при помощи уравнения Фрейнддиха в области средних давлений. [37]
В общем случае, по-видимому, можно утверждать, что при ван-дер-ваальсовой адсорбции скорость адсорбции молекул газа определяется той скоростью, с которой они могут достичь поверхности. Медленные процессы являются следствием хемосорбции, химической реакции, растворения или наличия препятствий, мешающих молекулам входить в соприкосновение с поверхностью адсорбента. [38]
Неоднородность поверхности адсорбента сказывается значительно больше при хемосорбции, чем при ван-дер-ваальсовой адсорбции. Влияние неоднородности на хемосорбцию будет детально обсуждаться во II томе; здесь же мы поясним это на двух примерах. Во-первых, Брунауер и Эммет [41] нашли, что если часть поверхности железного катализатора покрыта слоем кислорода, то физическая адсорбция азота ( или любого другого газа) происходит одинаково легко как на части поверхности, покрытой кислородом, так и на неокисленных атомах железа, хемосорб-ция же водорода или окиси углерода исключена на окисленной части и протекает лишь на атомах железа. Если вся поверхность покрыта кислородом, хе-мосорбция водорода при - 78 или окиси углерода при - 183 почти полностью исключена, на физическую же адсорбцию азота окисление поверхности практически не оказывает влияния. [39]
Кроме таких пограничных случаев, как адсорбция азота окисью хрома, теплоты ван-дер-ваальсовой адсорбции и хемосорбции обычно легко различимы. Дальнейшие интересные примеры были найдены в случав теплот адсорбции водорода на различных металлических и окисных катализаторах. За исключением измерений Эммета и Гаркнеса, приведенные выше теплоты хемосорбции и ван-дер-ваальсовой адсорбции не были определены на одном и том же адсорбенте. Однако теплоты ван-дер-ваальсовой адсорбции водорода, вероятно, не сильно изменяются для различных образцов меди и железа. [40]
Кроме таких пограничных случаев, как адсорбция азота окисью хрома, теплоты ван-дер-ваальсовой адсорбции и хемосорбции обычно легко различимы. Дальнейшие интересные примеры были найдены в случае теплот адсорбции водорода на различных металлических и окисных катализаторах. За исключением измерений Эммета и Гаркнеса, приведенные выше теплоты хемосорбции и ван-дер-ваальсовой адсорбции не были определены на одном и том же адсорбенте. Однако теплоты ван-дер-ваальсовой адсорбции водорода, вероятно, не сильно изменяются для различных образцов меди и железа. [41]
Дисперсионный эффект был введен в вычисление теплот адсорбции Лондоном [8], который возражал против объяснения ван-дер-ваальсовой адсорбции притяжением между постоянными диполями молекул газов и электрическими зарядами на поверхности на том основании, что такая картина сделала бы необходимой перемену знака силы взаимодействия каждый раз, как только молекула передвинулась бы от одной точки поверхности к соседней. Это должно было бы значительно уменьшить подвижность молекул вдоль поверхности в противоречие общепринятому взгляду, что при физической адсорбции молекулы обладают свободной подвижностью по поверхности. Доказательство свободного движения было дано при обсуждении потенциальной теории в гл. V, а именно - было указано, что уравнению состояния газа подчиняется также и адсорбционная фаза. Другое доказательство было предложено Фольмером и Ади-кари [ 2в ], которые экспериментально доказали подвижность адсорбированных молекул, как это будет показано в гл. Эти факты указывают на важность дисперсионных сил в адсорбции, так как эти силы всегда являются силами притяжения и не меняют своего знака с перемещением молекулы по поверхности. [42]
Как показывают эти результаты, теплоты хемосорбции кислорода на угле в двадцать-пятьдесят раз больше теплот ван-дер-ваальсовой адсорбции. Имеются другие системы адсорбент - адсорбируемое вещество, которые проявляют почти столь же большое различие, как и система уголь - кислород. [43]
Хотя в настоящее время мы практически не обладаем информацией об относительном значении обсуждавшихся факторов в ван-дер-ваальсовой адсорбции, можно попытаться в заключение сделать некоторые предварительные выводы. [44]
Дисперсионный эффект был введен в вычисление теплот адсорбции Лондоном [8], который возражал против объяснения ван-дер-ваальсовой адсорбции притяжением между постоянными диполями молекул газов и электрическими зарядами на поверхности на том основании, что такая картина сделала бы необходимой перемену знака силы взаимодействия каждый раз, как только молекула передвинулась бы от одной точки поверхности к соседней. Это должно было бы значительно уменьшить подвижность молекул вдоль поверхности в противоречие общепринятому взгляду, что при физической адсорбции молекулы обладают свободной подвижностью по поверхности. Доказательство свободного движения было дано при обсуждении потенциальной теории в гл. V, а именно - было указано, что уравнению состояния газа подчиняется также и адсорбционная фаза. Другое доказательство было предложено Фольмером и Ади-кари [29], которые экспериментально доказали подвижность адсорбированных молекул, как это будет показано в гл. Эти факты указывают на важность дисперсионных сил в адсорбции, так как эти силы всегда являются силами притяжения и не меняют своего знака с перемещением молекулы по поверхности. [45]
Страницы: 1 2 3 4