Атомная фаза
Cтраница 1
Атомная фаза обладает наибольшей валентной ненасыщенностью, наибольшей поверхностной энергией и может проявлять высокую каталитическую активность, если по термодинамическим условиям ее образование и существование возможно в условиях катализа. [1]
Роль атомной фазы в катализе была уже подмечена Тайлором [6], который говорил о преимущественной активности наиболее ненасыщенных пиковых атомов решетки. [2]
Активность атомной фазы на носителях подтверждена при помощи нанесения гомогенных катализаторов на гетерогенные носители. [3]
Таким образом, если атомная фаза всегда активна, как таковая, то кристаллическая фаза является лишь активирующим фактором, причем только в определенных случаях и при определенных условиях. [4]
Рентгеновский метод не констатирует атомную фазу, но он способен указать верхнюю границу дисперсности ( 10 А) и нерегулярность колебания атомов в кристалле. [5]
Это значит, что на поверхности катализатора должна быть атомная фаза. [6]
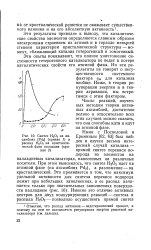 |
Синтез Н202 на ансамблях [ Pd2 ] ( кривая 1 и распад Н2О2 на кристаллической фазе палладия ( кривая 2. [7] |
При этом выяснилось, что синтез Н2О2 идет на атомной фазе ( на ансамблях Pd2), а разложение - на кристаллической. [8]
При нагревании катализатора до 600 мелкие кристаллы практически полностью диспергируют и количество атомной фазы возрастает до а ( 1 - РН. [9]
Оно показало, что для объяснения взаимодействия нанесенного ферромагнетика необходимо допустить присутствие на поверхности его атомной фазы как передатчика обменного взаимодействия. [10]
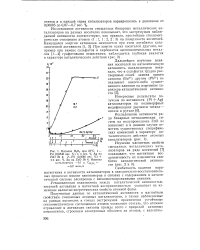 |
Катализ Н2О2 при 25 С. 1. [11] |
Установленная взаимосвязь между каталитической активностью, энергией активации и магнитной восприимчивостью указывает на изменение валентно-энергетических свойств атомной фазы. [12]
Адсорбированные на поверхности ионы серебра и восстановленные традиционным способом с помощью водорода при повышенных температурах до атомной фазы, как это принято в катализе, не дают спектра ЭПР атомов, что можно объяснить предположением о большой активности атомов при столь высоких температурах. [13]
Грязное в своем выступлении полемизировал с В. П. Лебедевым и указал, что хотя возможность протекания каталитической реакции на атомной фазе у большинства работающих в области катализа не вызывает сомнения, но и нет никаких прямых доказательств, что, правильно образованный кристалл будет неактивен. [14]
Это явление с позиций термодинамики было рассмотрено О. П. Полтораком, который исходил из следующей модели: активные центры являются атомной фазой, адсорбированной на поверхности кристалла. При этом оказалось, что для мелкодисперсных кристаллов количество атомной фазы на единицу поверхности уменьшается с ростом кристаллов. Таким образом, с изменением температуры протекают два конкурирующих процесса: сначала при повышении температуры обработки катализаторов увеличивается число дефектов, а следовательно, и их поверхностная концентрация; при дальнейшем повышении температуры увеличение числа дефектов и их подвижности приводит к росту кристаллов, а следовательно, к уменьшению поверхностной концентрации дефектов. [15]
Страницы: 1 2 3 4